はじめに
肥満の治療や予防では、食事療法や運動療法を中心とした生活習慣の改善が基本とされていますが、それらで短期的な体重減少が得られても、リバウンドが問題となることが少なくありません。その背景には、単に「食べ過ぎる」「運動が続けられない」といった行動面だけでなく、ストレスや不安、気分の落ち込み、疲労による自制力低下といった心理的要因も大きく関与していると指摘されています(文献1)。
近年、こうした課題への新たな解決策として、第3世代の認知行動療法(Third-Wave Cognitive Behavioral Therapy:3wCBT)が注目されています。3wCBTにおける従来のやり方との大きな違いは、不安や落ち込みといった「嫌な感情」を無理に消そうとしたり、抑え込んだりしない点にあります。そうした感情を自分の一部として受け入れながら、それでも「自分が本当に大切にしたい行動」を選び取っていく力(心理的柔軟性)を養うのが、この療法の目指すゴールです(文献2)。
本稿で紹介していくマインドフル・イーティング(Mindful Eating)は、この考え方を食事の仕方に応用した方法です。食事にしっかりと意識を向け、「お腹が空いた」「満腹だ」といった感覚を敏感に感じ取れるようになることで、「無意識の食べ過ぎ」や「習慣的な過食」を抑える効果があると考えられています(文献3)。
マインドフル・イーティング(Mindful Eating)とは
マインドフルネスとは、「今この瞬間の体験に、良し悪しの判断をせず、ありのまま意識を向けること」を指します。これを食事に当てはめたのがマインドフル・イーティングです。つまり、「今食べていること」そのものに集中し、「これは太るからダメだ」「食べ過ぎてしまった」といったジャッジ(価値判断)を脇に置いて、食事の体験をありのままに感じる姿勢を大切にしています。

マインドレスな食行動とその影響
現代の生活では、次の予定を考えながら食事をしたり、テレビやスマートフォンを見ながら食べたりする、いわゆる「ながら食べ」が日常化しやすくなっています。その結果、私たちの注意は食事中であっても食事以外のものへと注意が分散し、味や食感、満腹感といった身体のサインを十分に感じ取れない「マインドレス」な状態に陥りがちです。このような状態では、必要以上の量を摂取してしまうといわれています。
マインドレスな状態は、食べる量だけでなく、食事の選択にも影響します。例えば、身体的に空腹ではないにもかかわらず、口寂しさやストレス、疲労感などをきっかけに食べてしまうことがあります。また、「今なら◯◯が無料」「大盛りまで追加料金なし」といった外的刺激に反応し、すでに満腹に近い状態であっても、つい過剰に食べてしまう場面も少なくありません。
このような食べ方は、意識が現在の体験(今の満腹感など)から離れてしまい、特定の状況に反応して無意識に体が動く「オートパイロット(自動操縦)」の状態になっていることが原因の一つと考えられています。
マインドフル・イーティングの考え方
マインドフル・イーティングでは、こうした自動的な食べ方に気づき、今この瞬間の食事体験に意識を向けることを重視します。医学的な必要性がない限り、特定の食品を禁止したり、カロリーを制限したりすることは行いません。その代わりに、「本当に必要なものを、必要な量だけ、意識的に味わって食べる」ことを目標とします。
具体的には、ストレスや寂しさといった内的要因や、広告や割引などの外的要因に流されるのではなく、自身の空腹感に注意を向け、「本当に空腹なとき」に食べるようにします。食事の際には、香り、味、食感などを、五感を使って一口一口丁寧に味わうことで、「食べた」という実感や満足感が得られやすくなります。その結果、自然と食事のペースが落ち、食べ過ぎる前に無理なく箸を置けるようになることが少なくありません。
「満足感」を育てるという視点
マインドフル・イーティングの特徴は、食べる量をあらかじめ制限するのではなく、「満足感を育てること」から始める点にあります。この考え方は、食事制限に伴う心理的な負担を軽減し、行動変容を継続しやすくする利点があると考えられています。
また、私たちが感じる「空腹感」の中には、エネルギー不足による実際の身体的空腹によるものではなく、ストレスや不安、孤独感などを空腹と誤って認識している場合があります。「心の飢え」と言ってもよいかもしれません。そのため、マインドフル・イーティングでは、今感じている空腹感が、身体的な真の空腹によるのかどうかを見極める力を養うことや、食べ物以外の方法で心を満たす工夫を身につけることも重要な要素として位置づけられています。
具体的な実践方法
マインドフル・イーティングは、特別な道具や準備を必要とせず、日々の食事の中で少しずつ身につけていくことができます。実際の生活では、食事のすべてを変えるのではなく、「一部を残す」「途中で箸を置いて満腹感を確認する」といった小さな工夫から始めることが現実的です。詳細は拙書(文献4)にて紹介しています。瞑想のエクササイズに関しては、下記の動画も参考になるかもしれません。
慶應義塾大学病院での取り組み
慶應義塾大学病院では、腎臓・内分泌・代謝内科と精神・神経科が連携し、マインドフル・イーティングを取り入れた診療を行っています。2026年2月からは、不定期ではありますが、集団療法としての提供も開始しています。ご関心のある患者さんは、まずは肥満症外来の担当医にご相談ください。
外来担当医一覧
土曜日午前初診:山市大輔(精神・神経科)
集団精神療法担当:横山貴和子(精神・神経科)
参考文献
- Impact of a Mindfulness Mobile Application on Weight Loss and Eating Behavior in People with Metabolic Syndrome: a Pilot Randomized Controlled Trial.
Matsuhisa T, Fujie R, Masukawa R, Nakamura N, Mori N, Ito K, Yoshikawa Y, Okazaki K, Sato J.
Int J Behav Med. 2024 Apr;31(2):202-214. doi: 10.1007/s12529-023-10173-2. Epub 2023 Mar 21. - “Third-wave” cognitive and behavioral therapies and the emergence of a process-based approach to intervention in psychiatry.
Hayes SC, Hofmann SG.
World Psychiatry. 2021 Oct;20(3):363-375. doi: 10.1002/wps.20884. - Mindfulness-Based Eating Awareness Training (MB-EAT) for Binge Eating: A Randomized Clinical Trial.
Kristeller J, Wolever RQ, Sheets V.
Mindfulness. 2014;5(3):282-297. doi:10.1007/s12671-012-0179-1. - マインドフルネス・ダイエット : 頑張らないから痩せていく / 山市大輔,横山貴和子 東京 : 金剛出版, 2024
うつ病と反復経頭蓋刺激療法(rTMS療法)
精神疾患の中でもうつ病は非常に有病率が高く、先進国を中心とした社会のストレス化からその罹患数は年々増加しております。その高い罹患率に加えて、個人および社会にかかる負担の大きさ、約3人に1人が十分な抗うつ薬での治療を行っても改善がみられないという難治性を示すという点から、世界保健機関はうつ病を、「社会を最も消耗させる疾患」の一つと位置付けています。
このような中、薬物治療および心理療法とは異なる新たな治療として、反復経頭蓋刺激療法(rTMS療法)が注目を集めるようになりました。日本では2019年に保険収載され、KOMPASでも2020年に紹介いたしました(反復経頭蓋刺激療法(rTMS療法) ~お薬が効かないうつ病への新たな治療選択~ ―精神・神経科―)。保険収載をされてからの5年間の歳月でその長所と短所がより明確化されました。そして世界ではその短所を克服すべく、rTMS療法を発展させた治療法が、アメリカ食品医薬品局(FDA)にて承認されています。今回は、日本で行われているrTMS療法の現状と、世界でどのような発展がみられているかについて紹介します。
日本におけるrTMS療法の現状
rTMS療法は、脳の局所に反復的に磁気刺激を行うことで、神経可塑性(脳内の神経の柔軟さ)に変化を加えることで抗うつ効果を来す治療法です(図1)。一日40分のセッションを、週5日、3週間から6週間にわたって行います。rTMS療法の特徴は大きく2点あり、(1)難治性うつ病の方に対しても一定の抗うつ効果がみられることと、(2)従来の治療法と比べ、副作用が少ないことがあります。そのため、薬物治療に対して抵抗性および不耐性のあるうつ病の方に適した新しい治療選択として注目をされています。
日本ではrTMS療法が保険収載をされて、2024年6月で5年の歳月が経ちます。しかし残念ながらまだ本治療は一般化されていません。その原因として、厳しい施設基準や医療費の問題に加え、実施にかかるコストも大きな問題となっております。基準を満たした有資格者のみ実施可能であり、一人の治療に前後の準備も含め約60分程度かかること、一人の患者さんを治療するに当たり最大30日の日数がかかることが挙げられます。これは患者さん、そして医療従事者の双方の大きな負担となります。また上記に加えて、治療反応率が最大でも5割程度に限られること、適応が急性期治療(症状を改善させることを目的とした治療)に限られることもrTMS療法の普及を妨げる要因となっております。
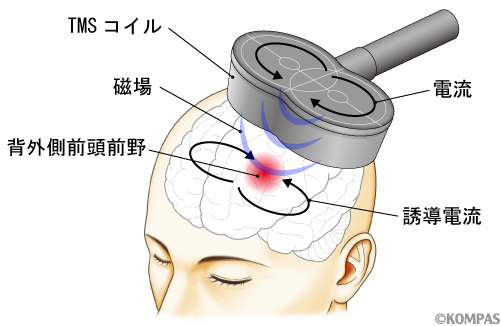
図1.TMSによる脳の局所刺激
rTMS療法の発展
世界および日本の一部の医療機関では、上記の短所を解決するためにrTMS療法をさらに発展させた新たな治療法が開発されております。本記事では、治療の時間的コストを解消する治療法、治療の効果を高める治療法、再発予防法といった、rTMS療法の3つの発展を紹介させていただきます。
時間的コストの改善 ~DASHプロトコルとシータバースト刺激~
rTMS療法における刺激の繰り返し方を発展させ短時間で同等の効果を来す手法が開発されております。DASHプロトコルは従来のrTMS療法のインターバルを減らすことで治療時間を約半分に、シータバースト療法はシータリズム(1秒に5回)でバースト刺激(20ミリ秒間隔の3連刺激)という特殊な刺激を行うことで一回の治療をわずか3分程度に短縮させたものです。日本ではまだ保険収載はされていないものの(治療機器の薬事承認はされているため一部の医療機関で自由診療や臨床研究として行われている場合はございます)、米国ではFDAで承認され一般的に行われるようになりました。時間的コストの改善は患者さんと、医療従事者の双方に大きな利点があるため日本でも早期に保険収載されることが期待されます。
治療効果の改善 ~SAINTプロトコル~
スタンフォード大学で開発された新しい治療です。SAINTプロトコルは、一日10時間の治療(10分間の刺激と50分の休憩を10セット)を5日間行うものであり、特殊なMRIを用いた治療部位の選定を行います。5日間と治療期間は短いものの、一日当たりの長い治療時間やMRIの撮像を要することから、治療にかかるコストは従来のものと比べて高まります。しかしこの集中的な治療は治療反応率8割という非常に高い効果を示しました。米国では2022年にFDA承認されたものの、治療にかかるコストや技術の問題から一般的には行われていません。また臨床研究の数も限られており、その効果の検証も不十分といった懸念点もあります。しかしながらその高い効果と、短い治療時間から、今後の世界的な普及が注目されております。
再発予防 ~メンテナンスrTMS~
rTMS療法は主に急性期治療として用いられることがほとんどでした。しかしながらうつ病の管理では、再発の予防も大事な要素となります。急性期治療としてのrTMS療法は、週5日の治療を要するため再発予防の手段としては適しておりませんでした。しかし、世界ではその治療頻度を抑えたうえで再発予防効果を来すメンテナンスrTMS療法が開発されています。日本でも国立精神・神経医療研究センターを中心として先進医療Bとして行われております。
おわりに
rTMS療法はまだ世界的にも新しい治療であり、上記で紹介したものに限らず世界中で常に新たな発展が試みられております。本治療を必要とされる患者さんに一日でも早く届けられれば幸いです。
うつ病と治療抵抗性
うつ病は、抑うつ、意欲低下、不安などを特徴とする、最も有病率の高い精神疾患の一つで、15人に1人はうつ病に罹患するともいわれております。特に先進国では社会のストレス化から、うつ病に罹患する患者さんの数は年々増える一方です。世界保健機関(World Health Organization: WHO)は、その社会保障費の増大、Quality of life (QOL)の低下、そして個人あるいは社会に対する間接的な負担が大きいことから、うつ病を「社会を最も消耗させる疾患」の一つと位置付けています。
うつ病に対する基本的な治療として、休養、心理療法、および環境調整を行いますが、それでも改善が見られない患者さんには薬物療法を行います。
しかしながら50%以上のうつ病患者は最初の抗うつ薬で寛解には至らず、3人に1人は2種類以上の抗うつ薬を十分量・十分期間の治療を行っても十分な改善が得られない治療抵抗性うつ病とされております。また、薬物治療への副作用から、治療の継続が困難となる患者さんもいらっしゃいます(治療不耐性うつ病)。このような背景から、うつ病に対する新たな、副作用の少ない治療法を確立することが強く求められています。
反復経頭蓋刺激療法(rTMS療法)とは
治療概要
反復経頭蓋磁気刺激療法(repetitive Transcranial Magnetic Stimulation: rTMS療法)とは、2019年6月に保険収載された、うつ病の新たな治療法です。反復的に磁気刺激を行うことで、神経可塑性(脳内の神経の柔軟さ)に変化が加わり、抗うつ効果を来すとされています。アメリカでは2008年に、アメリカ食品医薬品局(Food and Drug Administration :FDA)に承認されており、世界的には標準治療の一つとされております。
rTMS療法の特徴は大きく2点あり、(1) 治療抵抗性うつ病の方に対しても一定の抗うつ効果が見られること、(2) 従来の治療法と比べ、副作用が少ないことがあります。そのため、薬物治療に対して抵抗性及び不耐性のあるうつ病の方に適した新しい治療選択として注目をされています。また毎日外来に通院して治療を受けるという枠組みから、生活習慣の改善や復職準備性の向上といった、患者さんのQOL改善にもつながりやすい特徴も兼ね備えています。
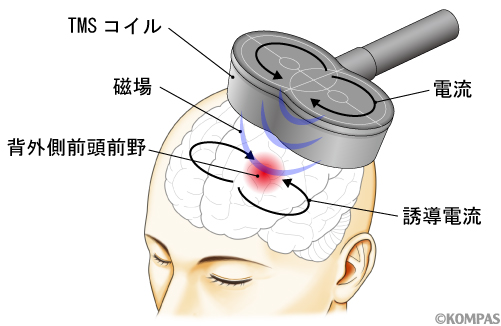
図1.TMSによる脳の局所刺激
治療内容
rTMS療法では、1日40分のセッションを、週5日、3週から6週間にわたって行います。週5回の通院を要するため、上述の通り患者さんの行動活性化や生活習慣の改善などにつながる一方で、通院が負担になってしまう方も多くいらっしゃいます。その場合は入院をしながらrTMS療法を行うケースもあります。
専用のコイルを頭に当てることで治療を行います。コイルに瞬間的に電流が流れると磁場が発生し、その磁場が変動するとファラデーの法則により微弱な誘導電流が生じます。rTMS療法では局所的に渦電流を発生させることができる特殊なコイルを用います。そのため目的部位以外を刺激してしまうことはありません。
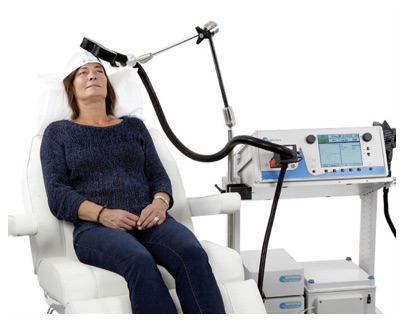
図2. rTMS療法の実際の様子
(出典:インターリハ株式会社のサイトより使用許諾を得て掲載)
効果および安全性
効果については、3~5割程度のうつ病患者さんの症状の改善が認められます。一見すると低いように思われますが、これは「治療抵抗性うつ病」の方に効果が認められる割合となります。再発率に関するデータは十分ありませんが、rTMS療法が有効であった患者さんの6~12ヶ月における再発率は1~3割と推定されています。
比較的頻度の多い副作用として知られているのは、頭皮痛・刺激痛、顔面の不快感、頸部痛・肩こり、頭痛です。これらのほとんどが刺激中に限定した副作用で、治療後まで持続することは基本的には少ないです。しかしまれに刺激が終わってからもこれらの違和感が残存することがあります。重篤な副作用として知られるのは、頻度は高くはありませんが、けいれん発作が挙げられます。けいれん発作そのものは自然に終息しますが、けいれん発作に伴う外傷や嘔吐物誤嚥などの危険性が想定されます。これまでのrTMSに起因する全てのけいれん誘発事例の報告の中で、けいれんを繰り返す症例や、てんかんを新たに発症した症例は1例も報告されていません。また、抗うつ薬によるけいれん誘発の危険率と比較してもrTMS療法が特別そのリスクが高いわけではありません。
慶應義塾大学病院での治療の特徴
慶應義塾大学では、臨床研究(UMIN000028855)の枠組みで行う場合、刺激部位のMRIナビゲーションを行います。脳構造は個人個人によって異なることが知られており、経頭蓋から正確に刺激部位である背外側前頭前野を刺激することは困難です。そこで当院では事前にMRI画像の撮像を行い、それを基にした刺激部位のナビゲーションを行うことで、刺激部位の正確な刺激を実現します。上記の治験にご関心のある方は、詳細をご説明申し上げますので、以下のフォームよりお申し込みください。
・うつ病に対するrTMS治療縦断研究(慶應義塾大学医学部精神・神経科学教室)
今後の展望
rTMS療法はTMSによる刺激を反復することを意味しますが、その反復の仕方には非常に発展性があります。神経可塑性をより強く誘導するTheta burst stimulation、個々人の脳波反応に合わせたsynchronized rTMS療法、functional MRIによる機能的結合性を元に刺激部位を決定するfMRIガイド下rTMS療法など、その治療効果を高める研究は日々行われております。そのため、我々はより短時間でかつ効果的なrTMS療法の開発に取り組んでおります。

左から:野田賀大(精神・神経科特任講師)、筆者(同助教(臨床実習))
治療抵抗性統合失調症の治療
統合失調症治療の中心は半世紀前に発見されたドパミン受容体拮抗作用を持つ抗精神病薬で、統合失調症のドパミン機能異常仮説の根拠となっています。統合失調症の陽性症状(幻覚や妄想)に対し、約3割の患者さんでドパミン受容体拮抗薬(従来の抗精神病薬)は無効です。
クロザピン(商品名:クロザリル)は、2種類以上のクロザピン以外の抗精神病薬で十分な治療効果を得られない治療抵抗性統合失調症に対して有効であることが確立されている唯一の薬剤です。治療抵抗性統合失調症は、反応性不良統合失調症と耐用性不良統合失調症の2つに分けられます。
反応性不良統合失調症とは、忍容性に問題がない限り、2種類以上の十分量の抗精神病薬(クロルプロマジン換算600mg/日以上で、1種類以上の非定型抗精神病薬を含む)を適切な服薬コンプライアンスで十分な期間(4週間以上)服薬しても反応が認められなかった統合失調症と定義されています。ここで、反応の有無はGlobal Assessment of Functioning(GAF)という評価尺度を用いて評価します。
耐用性不良統合失調症とは、非定型抗精神病薬のうち、2種類以上による単剤治療を試みたが、(1)中等症以上の遅発性ジスキネジア、遅発性ジストニア、あるいはその他の遅発性錐体外路症状の出現、または悪化、または、(2)コントロール不良のパーキンソン症状、アカシジア、あるいは急性ジストニアの出現のために、十分に増量できず、十分な治療効果が得られなかった統合失調症と定義されています。これらの症状は、Drug-Induced Extrapyramidal Symptoms Scale(DIEPSS)という評価尺度を用いて評価します。
クロザピンは、治療抵抗性統合失調症に対し、有効性の基準によるものの、30%から60%に有効とされています。クロザピンは、難治性の陽性症状だけでなく、衝動性、自傷・他害にも有効で、治療継続率を上げ、入院期間を減少させます。一方、他の抗精神病薬よりも副作用に注意が必要で、重大な副作用((1)無顆粒球症好中球減少症、白血球減少症、(2)高血糖、糖尿病性ケトアシドーシス、糖尿病性昏睡、(3)心筋炎、心筋症、心膜炎、心のう液貯留)が起こる可能性もあります。そのため、クロザピン導入は血液内科医や糖尿病内科医との連携が円滑な入院環境で行われなければならず、用量の調整も非常に緩徐に増量していくことが定められています。しかし、治療抵抗性統合失調症と診断されてからクロザピン導入までの期間が短いほど、臨床効果が高い、という報告が複数あり、早期のクロザピンの開始が望まれます。
クロザピン専門外来
慶應義塾大学病院精神・神経科外来では、2016年10月より、毎週火曜日(午前)にクロザピン外来を開始することとなりました(担当医師 中島振一郎)。統合失調症の患者さんの中で、これまで服薬されてきたお薬の効果が十分ではない方、または、対応の難しい副作用のため、十分に服用ができなかった方に対して、クロザピンによる治療が適切かどうか、患者さん自身やご家族と一緒に医師が相談させていただき判断する外来です。
具体的には、治療歴・既往歴・家族歴の確認、評価尺度や検査を用いた統合失調症状の包括的な評価を行い、治療抵抗性統合失調症(反応性不良統合失調症または耐用性不良統合失調症)かどうかを判定します。また、身体状況の精査(歯科依頼、血液検査、心エコー、脳波、心電図、腹部X線)、クロザピンに対する禁忌の確認を行います。
クロザピンによる治療が適切とされた場合には、前の項で記しましたクロザピン治療によるリスクとベネフィットと入院による導入の方法について、文章と口頭にて丁寧に説明いたします。重症度、地理的条件、支援体制にもとづいて、当院またはクロザピン導入が可能な他院における治療の開始を検討いたします。受診希望の方は紹介状を準備の上、病院の初診予約センター![]() よりご予約ください。
よりご予約ください。
治療抵抗性統合失調症に関する臨床研究
統合失調症治療の中心は半世紀前に発見されたドパミン受容体拮抗作用を持つ抗精神病薬で、統合失調症のドパミン機能異常仮説の根拠となっています。しかし、統合失調症の陽性症状に対し、約3割の患者さんで従来の抗精神病薬は無効です。更に、最近の研究によりますと、治療反応性統合失調症ではドパミン生成能が亢進していますが、治療抵抗性統合失調症ではドパミン生成能の亢進を認めません。故に治療抵抗性統合失調症は従来のドパミン仮説では説明できません。
一方、グルタミン酸仮説は治療抵抗性統合失調症の病態を説明する仮説として有力です。グルタミン酸仮説は陰性症状(表出や意欲の低下)や認知機能障害も説明する可能性があり、ドパミン仮説より包括的な仮説とされています。近年、プロトン核磁気共鳴スペクトロスコピー(1H-MRS)という核磁気共鳴イメージング(MRI)技術の発展により脳内グルタミン酸を測定することが可能になりました。
1H-MRS研究によりますと、一貫して、初発統合失調症では線条体グルタミン酸濃度が高いことが報告されています。こうした背景から、グルタミン酸仮説に基づいた薬剤開発が現在進められています。しかし、統合失調症における抗精神病薬による治療反応性と線条体グルタミン酸の関係は不明です。更に、グルタミン酸は脳内ネットワーク結合性に不可欠な役割を担っていますが、統合失調症における抗精神病薬による治療反応/治療抵抗性の基盤となる脳内の構造的・機能的結合性とグルタミン酸の関係は不明です。
そこで、慶應義塾大学医学部精神・神経科学教室では、マルチモーダルMRIを用いて治療抵抗性統合失調症の生物学的機序を解明することを目的に、臨床研究![]() を行っています(主任研究者 中島振一郎)。具体的には、年齢・性別・抗精神病薬をマッチした治療抵抗性統合失調症患者さん、治療反応性統合失調症患者さん、健常人における線条体グルタミン酸濃度や機能的・構造的結合性の測定と比較を行い、治療抵抗性の臨床症状・認知機能の神経基盤(機能的・構造的脳内結合性)におけるグルタミン酸の役割の解明を目指します。
を行っています(主任研究者 中島振一郎)。具体的には、年齢・性別・抗精神病薬をマッチした治療抵抗性統合失調症患者さん、治療反応性統合失調症患者さん、健常人における線条体グルタミン酸濃度や機能的・構造的結合性の測定と比較を行い、治療抵抗性の臨床症状・認知機能の神経基盤(機能的・構造的脳内結合性)におけるグルタミン酸の役割の解明を目指します。
本研究の意義は、治療抵抗性統合失調症についてグルタミン酸受容体介在型神経系の観点から新たな生物学的機序を発見し、統合失調症という疾患概念において、既存の薬剤に反応するドパミン系異常群と、治療抵抗性であるグルタミン酸系異常群を層別化し、グルタミン酸系神経機能の異常を焦点とした新たな治療法の開発に繋げていくことです。本研究が治療抵抗例に対するグルタミン酸系薬剤の開発に寄与し、そして、既存の薬剤が無効な症状からの回復と社会復帰を促進することを期待しております。

筆者

