慶應発サイエンス
大腸がんに対する薬の効果を予測するオルガノイド培養技術を開発 〜正常な「ミニ臓器」の培養効率を飛躍的に改善〜
研究の背景
多数の治療薬候補の効果を網羅的に探索する薬剤スクリーニング(注1)は、がん創薬における基盤技術です。従来のがん創薬では患者がん組織から樹立したがん細胞株(注2)を用いて一次スクリーニングを行い、動物モデルを用いて安全性や副作用を確認するという手法をとってきました。
しかし、がん細胞株には、実際の臨床腫瘍の性質や抗がん剤への感受性の多くを欠落しているという問題点があります。また、がんはたとえ同じ臓器に発生しても患者さんごとに異なる遺伝学的、生物学的な特徴を示しますが、がん細胞株ではこの多様性を網羅できません。結果として、がん細胞株を用いて選別された抗がん剤候補の多くが臨床応用に至っておらず、この創薬研究における「死の谷」が大きな医学的および社会的問題となっています。
我々の研究グループは、患者組織を「ミニ臓器」として培養皿上で永続的に培養するオルガノイド技術(注3)を開発し、これまで大腸がん、胃がんをはじめとした多くのがんのオルガノイドバンクを構築してきました。患者由来がんオルガノイドは患者がん組織の特徴を多く保持しており、「生きた」がん組織からなるオルガノイドバイオバンクは次世代のがん研究リソースとして、がん基礎研究や診断ツール、創薬や個別化治療へ応用されようとしています。最近の海外の臨床試験では、患者由来がんオルガノイドの薬剤感受性と臨床腫瘍の抗がん剤への反応が相関することが示され、オルガノイドを用いて化学療法の治療効果を予測する「オルガノイド医療」の実現が期待されています。
しかしながら、オルガノイドを用いたこれまでの薬剤スクリーニングは、がん細胞株を用いた薬剤試験と同様に抗がん作用のみに焦点を当てており、正常組織に対する副作用や安全性を評価することは困難でした。オルガノイド技術を用いることで正常組織の培養が可能となりましたが、従来の培養技術では正常組織オルガノイドを安定的に大量培養することが難しく、薬剤スクリーニングに導入することができていませんでした。
研究の概要
ヒト大腸オルガノイドを用いた薬剤スクリーニングシステムの確立
大規模薬剤スクリーニングでは、多数の候補薬剤をさまざまな濃度で検討するため、事前に細胞を効率よく大量に培養する必要があります。また、ばらつきが少なく信頼性が高いデータを取得するためには、細胞あるいはオルガノイドが均等に育たなくてはなりません。従来のp38阻害剤を用いた培養法では、正常および一部のがんヒト大腸オルガノイドの単一細胞の解離後の回復が不十分であったためこれらの条件を満たすことができず、全てのオルガノイドを薬剤スクリーニングに用いることは困難でした。近年、我々はIGF-1とFGF-2という増殖因子を培地に添加することで、ヒト腸管オルガノイドの培養効率が飛躍的に向上することを報告しました。
本研究では、この培養条件を応用した浮遊培養技術を用いることで、内視鏡下生検検体に相当する少量の組織量から、正常ヒト大腸および大腸がん細胞を約1〜2か月の間に1,000万細胞まで安定的に増やすことが可能になりました(図1)。このシステムを利用して正常ヒト大腸オルガノイド6株とヒト大腸がんオルガノイド20株に対して56種類の薬剤を用いてスクリーニングを行い、高精度な薬剤感受性データを取得しました。
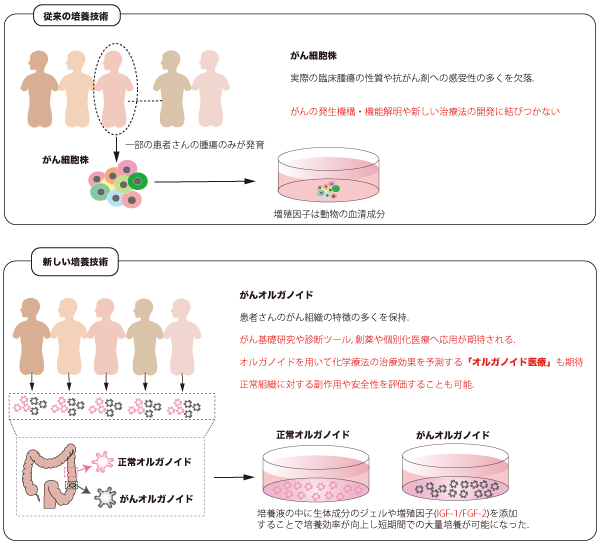
図1.患者由来オルガノイドを用いた新規薬剤スクリーニングシステムの開発
IGF-1とFGF-2という2つの増殖因子を加えることで、正常およびがんヒト腸管上皮オルガノイドの安定かつ効率的な大量培養が可能になった。
大腸がんに対してのみ効果を示す薬剤の探索
正常大腸オルガノイドと大腸がんオルガノイドの治療応答性を直接比較することで、正常細胞を傷害せず大腸がんに対してのみ効果を示す薬剤を探索しました。その結果、ブロモドメインタンパク質阻害剤である(+)-JQ1が、正常大腸オルガノイドに比べて大腸がんオルガノイドに対して強い効果を示すことを明らかにしました(図2)。また、トランスクリプトミクス分析により、(+)-JQ1は結腸直腸がんで異常に活性化される遺伝子発現を抑制することが明らかになりました。
ブロモドメインタンパク質阻害剤はスーパーエンハンサーを標的とすることが知られているため、本研究結果は、(+)-JQ1が発がん性依存性プログラムを抑制することによってがんオルガノイドの増殖を抑制したことを示唆しました。本研究結果はまた、潜在的な治療法の発見のために正常細胞を使用することの有用性も示しました。
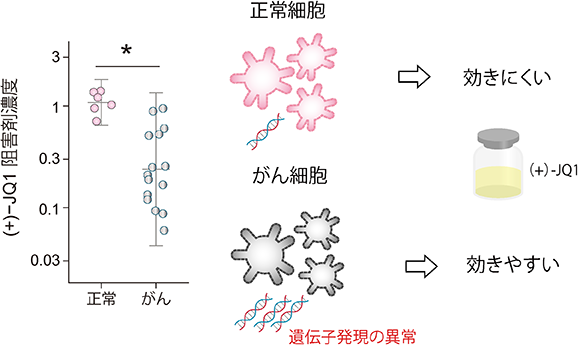
図2.BETブロモドメインタンパク質阻害剤の効果
ブロモドメインタンパク質阻害剤である(+)-JQ1は正常大腸オルガノイドと比較し大腸がんオルガノイドに強い効果を示す。
エピゲノム異常による治療応答性予測
がんでは多数の遺伝子異常が見られますが、同時に、遺伝子配列には異常をきたさない異常(エピゲノム異常)があることも知られています。大腸がんでは、約20%の症例において、CpG island methylator phenotype(CIMP)というエピゲノム異常が見られます。薬物反応の統合分析により、パクリタキセル感受性とCpGアイランドメチレーター表現型(CIMP)の間に有意な正の相関が検出されました。これは、BRAF変異とマイクロサテライト不安定性を伴う結腸直腸がんでよく見られます。 CIMP陽性がんの異種移植片は、一貫してパクリタキセルに対する感受性を示しました(図3)。本研究の結果は、乳がん、胃がん、卵巣がんなどのさまざまながんで臨床的に用いられる抗がん剤パクリタキセルのCIMP 陽性結腸直腸がん治療への転用の可能性を示唆しています。
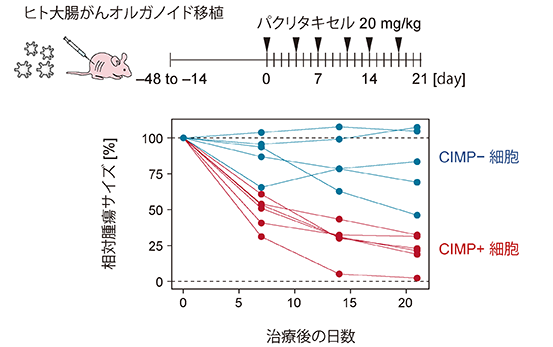
図3.CIMP陽性がんオルガノイドのパクリタキセル感受性
CIMP陰性がんと比較してCIMP陽性がんはパクリタキセルに対する感受性が高い。
本研究の成果と意義・今後の展開
本研究では、正常細胞を含む幅広い患者由来オルガノイドに適用可能な薬剤スクリーニングシステムを確立し、大腸がんにおける分子生物学的異常と複数の薬剤の治療応答性を結びつけることに成功しました。本研究により、患者由来オルガノイドを用いた薬剤スクリーニングのバイオマーカー解析における応用可能性が実証されました。本研究で開発された技術は、バイオマーカー研究および新規創薬研究に有用であり、基礎研究および創薬研究での幅広い応用が期待されます。
【用語解説】
(注1)薬剤スクリーニングシステム
現在医療で使用されている、または研究段階にある薬剤からがんを縮小する効果のある薬剤を選び出す手法。
(注2)がん細胞株
臨床検体から単一のがん細胞を単離して株化したもの。株化したがん細胞は、培養・維持が簡便かつ安価で実験に用いやすい。また、単一の遺伝背景に由来するため実験結果の再現が得やすく、遺伝子操作なども簡便に行える利点がある。ほぼ全てのがん種でさまざまな人種に由来するがん細胞株が樹立され、研究者間で譲渡されて使用されている。
(注3)オルガノイド技術
従来の培養技術では、体の細胞を平面状のシートにして培養・増殖させてきた。オルガノイド培養技術は、組織の細胞を立体的に培養し、体内の組織に近い状態に保つ培養技術。オルガノイド培養技術によって、ヒトのさまざまな組織(胃、小腸、大腸、乳腺、肺など)が培養可能になった。また、オルガノイド技術ががん細胞にも応用され、採取した患者がん細胞を体外で効率よく培養できるようになった。
参考文献
Organoid screening reveals epigenetic vulnerabilities in human colorectal cancer.
Toshimitsu K, Takano A, Fujii M, Togasaki K, Matano M, Takahashi S, Kanai T, Sato T.
Nat Chem Biol. 2022 Jun;18(6):605-614. doi: 10.1038/s41589-022-00984-x.

