慶應発サイエンス
新しいがんイメージングDIIFCO法の開発~がん微小環境を三次元レベルで解析可能に~
研究の背景
生体内でがんを取り巻く環境は、がんの成長に不可欠な栄養供給を支える血管や炎症細胞の浸潤に加えて、がん自身に起こる上皮間葉転換で、絶え間なく変化し続けています。上皮間葉転換とは、上皮細胞に由来するがん細胞がその特徴を変化させ、間葉系様の細胞に形態変化する現象です。この上皮間葉転換を介して、がん細胞は進行・転移します。
このようながんを取り巻く環境は「がん微小環境」と呼ばれ、抗がん治療に対する耐性化の原因とも考えられています。これを正確に理解することは、がん根絶を試みる基礎研究者にとって重要な課題です。さらにがん治療に従事する臨床医にとっては、治療予測を可能とするバイオマーカーにつながる可能性があります。
これまで、がん微小環境をミクロなレベルで可視化するための様々な顕微鏡や画像技術が開発されてきました。従来の顕微鏡では、得られた腫瘍組織を薄く切片に(2次元化)することで、タンパクおよび遺伝子の発現解析を行っていました。しかし、これでは組織断面を描画するだけの2次元イメージングに留まり、がん微小環境における3次元腫瘍情報の詳細を得ることができません。また、がん微小環境の分子機構をより正確に理解するために、病理学的な免疫組織染色法によるタンパクの局在解析に加えて 、分子生物学的なin situハイブリダイゼーション法によるRNAの局在解析も重要になっています。タンパクまで翻訳される遺伝子は、全遺伝子の1.5%に満たず、多くの発現遺伝子は細胞内にRNAとして存在し、癌微小環境の制御を行います。in situハイブリダイゼーション法は特異的なプローブを用いることで、RNAを検出する研究手法です。
しかし、in situハイブリダイゼーション法を施行するためには、RNAを包むタンパクを試薬で分解し、RNAを露出させる必要があります。この操作では、免疫組織染色とin situハイブリダイゼーション法の共存が難しいため、立体的な組織構造の維持が不可欠な3次元イメージング法を利用した1細胞レベルでのRNAとタンパクの同時解析を実現した研究はこれまでありませんでした。
研究の概要
本研究グループは、3次元ライトシート顕微鏡と組織透明化法と組み合わせることで、立体的な腫瘍空間に広がるタンパク/RNA発現の空間分布を1細胞レベルで解析可能にする、新規がんイメージングDIIFCO (Diagnosing In situ and Immuno-Fluorescence- labelled Cleared Onco-samples)法を開発しました(図1)。ライトシート顕微鏡とは、サンプルの側面からシート状の励起光を照射することで、光学断面像を得る次世代の蛍光顕微鏡です。深くまで照射できるシート状の励起光と光路を分けた検出レンズは、3次元像を得るために適しています。また、サンプルは溶媒の屈折率と一致することで透明になります。DIIFCO法では、組織を脱水・脱脂処理することで組織中の屈折率を均一化し、透明化処理を施します。今回、研究グループは、ライトシート顕微鏡に独自の免疫組織染色・in situハイブリダイゼーション法と組織透明化法を組み合わせ、標的分子のタンパクおよびRNAを発現する細胞を同時に検出し、がん組織の立体的な空間上に描画する世界初のがんイメージング法を確立しました。
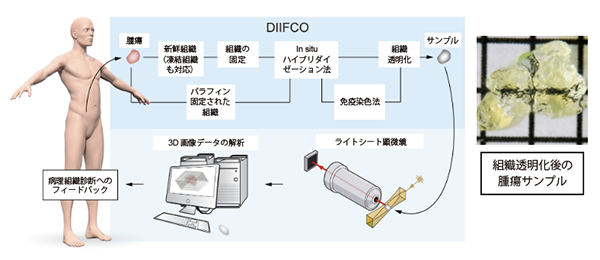
図1. DIFFCO法の概略
DIIFCO法で採用される新しいin situハイブリダイゼーション法では、RNAの検出にタンパク分解の必要性がなく、DIIFCO法で透明化される腫瘍塊では、免疫組織染色とin situハイブリダイゼーション法を同時に施行することができます。ライトシート顕微鏡を用いることで、組織塊の表面から深部まで解析範囲が広がり、標的分子の発現レベルに応じる3次元腫瘍マップが作成されます。がん微小環境の解析では、免疫染色される腫瘍血管と標的分子のRNAを持つ数百~数千万のがん細胞との位置関係が1細胞ごとに可視化され、不均一な脈管構造や上皮間葉転換の空間分布、さらには血管からの距離が、ミクロなレベルで可視化されます。このため、腫瘍空間でがん幹細胞が自らを育む環境(がん幹細胞ニッチ)も世界で初めて明らかになりました(図2)。ビデオは免疫染色で抽出された腫瘍血管(白色・線状)と癌幹細胞マーカーであるCD133陽性細胞(球)の位置関係が3次元で可視化されており、血管からの距離でCD133陽性細胞(球)が色分けされています。
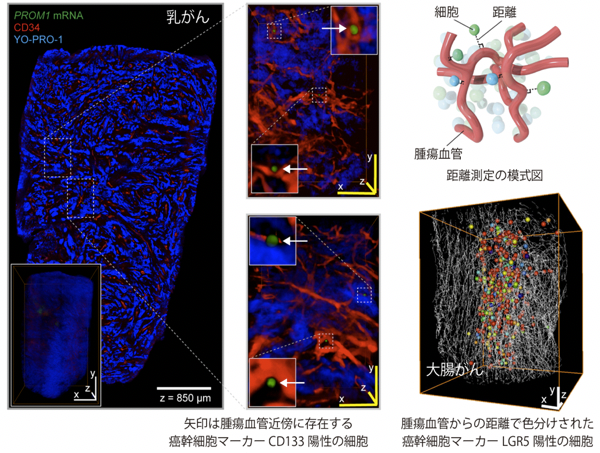
図2. DIFFCO法で明らかとなった細胞ニッチの詳細
図3. 癌幹細胞が生息する細胞ニッチの立体構造
*図1~3は参考文献のFigure 4Bより転載(一部改変)
本手法では、ホルマリン・パラフィン固定された保存サンプルを利用することが出来ます。つまり、DIIFCO法では病理診断後の組織やバイオバンクに存在する保存組織でも、1細胞レベルの高解像度なタンパク/RNAの同時発現解析を行うことが可能です。保存サンプルを活用できるDIIFCO法は、「ライトシート顕微鏡と組織透明化法の融合」を迅速化し、臨床現場への橋渡しを可能にする新規がんイメージングとして、将来の臨床応用が期待されます。
参考文献
Three-dimensional single-cell imaging for the analysis of RNA and protein expression in intact tumour biopsies.
Tanaka N, Kanatani S, Kaczynska D, Fukumoto K, Louhivuori L, Mizutani T, Kopper O, Kronqvist P, Robertson S, Lindh C, Kis L, Pronk R, Niwa N, Matsumoto K, Oya M, Miyakawa A, Falk A, Hartman J, Sahlgren C, Clevers H, Uhlén P.
Nature Biomedical Engineering 2020; 4: 875-888.

左より:筆頭著者の田中伸之(慶應義塾大学医学部泌尿器科学教室助教)、責任著者のPer Uhlén (スウエーデン、カロリンスカ研究所教授)

