慶應発サイエンス
脳梗塞における神経症状回復を促す新規免疫細胞の発見
研究の背景
脳血管障害(脳卒中)は日本人の死因の第3位で、年間11万人弱が死亡し、患者総数は100万人を超えています。脳卒中の中でも、脳の血管が詰まるなど血流が減少することによって、酸素や栄養が不足して脳組織が壊死に至る脳梗塞が約75%を占めています。脳梗塞は、死亡率が高いだけでなく後遺症が重く、患者さんの生活の質(QOL)が非常に低下します。発症後数時間以内の脳梗塞であれば、詰まった血管の再開通(血栓溶解または血栓除去)によって神経症状や後遺症の改善が期待できますが、そのような早期に発見できるケースは限られていて、それ以降の有効な治療法がほとんどありませんでした。しかし、脳細胞の死に伴って炎症反応が惹起され、炎症を制御することで脳梗塞の症状を緩和できることが明らかになってきました。
これまでの脳梗塞後の炎症に関する研究はマクロファージを中心とした自然免疫反応が中心でした。本研究グループでは、これまでに、マクロファージを中心とした脳梗塞発症後の炎症プロセスを明らかにしてきました(参照:KOMPAS慶應発サイエンス2017年10月掲載記事)。すなわち、発症1日目には炎症性のマクロファージが梗塞部位に浸潤し、死細胞由来の物質を認識して炎症性サイトカインを放出します。その後3日目にγδT細胞が浸潤しIL−17を放出して神経細胞死が亢進します。それ以降はマクロファージが修復性に転換し炎症物質を除去、およそ1週間で炎症反応が収束します (図1)。しかし、それ以降の慢性期においては炎症が収まっていると考えられてきたため、慢性期における免疫細胞の役割についてはほとんど解析されていませんでした。今回、我々研究チームは、マウス脳梗塞モデルを用いて梗塞発症後2週間以上経過した慢性期に制御性T細胞(Treg)(注1)が脳内に大量に集積することを見出しました(文献1)。
Tregは、転写因子(Forkhead box P3:Foxp3)を主要なマスター転写因子とし、自己抗原、共生細菌由来抗原、および外来抗原など多様な抗原に対して過剰な免疫応答を抑制し、炎症を抑える働きがあります。これまでの研究では、Tregが抑制する相手としては主に活性化されたエフェクターT細胞や樹状細胞、マクロファージなどが中心でした。しかし近年、定常状態および傷害時における非リンパ組織に存在するTreg細胞が注目を集めています(文献2)。それらは組織Tregと呼ばれ、組織に関わらず共通の性質を示すと同時に、それぞれの組織に特化した特徴も持っています(図2)。例えば、筋肉Tregは創傷治癒に寄与し、脂肪組織のTregは肥満によるインスリン抵抗性を抑制します。しかしこれまで脳内のTregは細胞数が非常に少なく、組織修復に関係する脳内Tregの存在は不明でした。
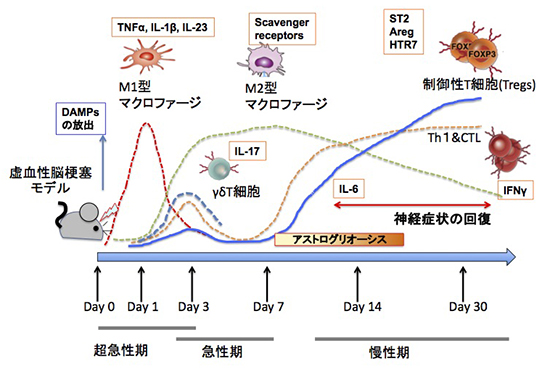
図1. 脳梗塞後の炎症に過程における浸潤細胞の時間経過
*細胞数は概念的なもので実測値ではない
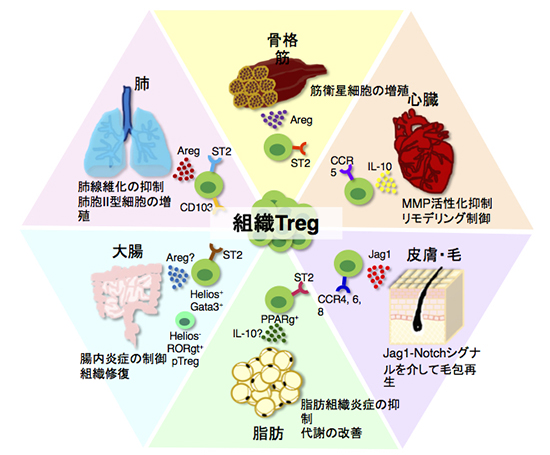
図2. 組織に局在する制御性T細胞(組織Treg)
脳梗塞における脳Tregの集積
実験的脳虚血再灌流(MCAO)モデル(脳梗塞モデル)(注2)では、発症2週目以降の慢性期にT細胞が集積することが見出されました。細胞を分画したところ、集積するCD4陽性T細胞のうちおよそ半数がFoxp3陽性の制御性T細胞でした(図3)。
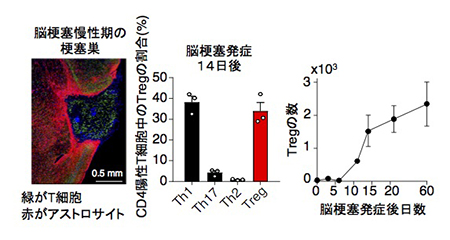
図3. 脳梗塞慢性期におけるT細胞、Treg細胞の脳内湿潤
まず、T細胞の浸潤の意義を明らかにするために、脳梗塞後慢性期にFTY720によってT細胞の集積を止めたところ、神経症状の悪化がみられました。さらに抗CD4抗体を投与し、CD4陽性T細胞を除去することでも神経症状が悪化しました。したがってT細胞、特にCD4陽性T細胞が脳梗塞後慢性期に神経症状の改善に寄与していることが分かりました。先に述べたように、CD4陽性T細胞の約半数がTregです。そこでさらに遺伝子操作によってTregを一過性に除去できるようにしたマウスを用いてTregを除去するとアストロサイトの活性化(アストログリオーシス)(注3)が起こり、神経症状が悪化しました(図4)。逆にRag欠損マウスやCD3ε欠損マウスのようなT細胞が存在しないマウスにTregを戻すと神経症状が改善されました。これらのことから脳梗塞慢性期には脳内にTregが大量に浸潤し神経症状の改善に重要な役割を果たしていることが示されました。
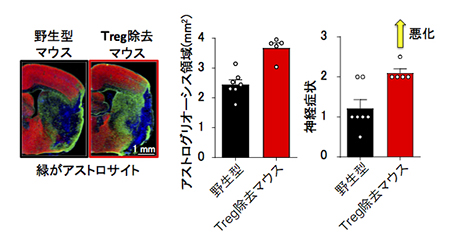
図4.
制御性T細胞(Treg)除去マウスではアストログリオーシスと神経症状の悪化がみられる。
脳Tregの性質
次に脳内に浸潤したTregの性質を解析しました。脳内のTregは、ほかの組織Tregと同様にHelios+の胸腺由来のTregであり、CTLA-4、PD-1、CD103、アンフィレグリン(Areg)、ST2(IL-33受容体 )を多く発現していました。また、脂肪組織Tregに似てPPARγを多く発現し、Tcf7とLef1の発現が低下していました。よって我々は脳梗塞後の慢性期に脳内に局在するTregを脳Tregと呼ぶことにしました。
まずTregは、脳内のみならず所属リンパ節でも増加していたことから何らかの特異的抗原を認識してクローナル増幅を行なっていると考えられます。そこで次世代シークエンサーおよびシングルセルによるPCRによってTCR遺伝子のレパトア解析を行いました。するとTCRβ遺伝子およびTCRα遺伝子(特にTCRα遺伝子)の使用に強い偏りがあることが見出されました。さらに抗原認識がTregの増加に必要であることを示すために、卵白アルブミンに対するTCRトランスジェニックマウスを用いたところ脳内でのT細胞の増加はほとんど見られませんでした。したがって脳内のTregは何らかの抗原を認識してリンパ節でクローン増幅を行なっていると考えられます。
また、脳梗塞後慢性期に脳内に局在するTregを単離し、別のマウスに移植して脳梗塞を起こすと、通常のマウス由来のTregよりも効率的に脳内に浸潤し増幅することが分かりました。そこで、脳Tregの増幅機構を調べました。IL−2はすべてのTregの生存、増殖で必須であり、抗IL−2抗体の投与によって脳Tregの数は減少しました。脳TregはIL−33受容体(ST2)を高発現することからIL−33の関与が示唆されました。そこでIL−33欠損マウス、ST2欠損マウスを調べたところ脳Tregの数は減少しました。よって脳Tregの増幅にはTCRシグナル、IL−2、IL−33が必須といえます。ちなみにIL−33の発現は脳梗塞によって増加し、オリゴデンドロサイトとアストロサイトが主な産生源です。IL-33を欠損するマウスは、修復性のM2マクロファージ関連遺伝子の誘導が減少し、神経損傷後の回復ができなくなることが報告されており、これらのIL−33の修復機能に脳Tregが関与する可能性は高いと考えられます。
次に、なぜ脳Tregは脳指向性なのかを調べました。通常リンパ球の組織への遊走にはケモカインとその受容体が関与します。Tregはケモカイン受容体のうちCCR6とCCR8を多く発現し、脳梗塞巣で上昇するCCL20やCCL1依存的に脳内に浸潤しました。逆にCCL20やCCL1を脳室投与するとTregが増加し、神経症状も改善されました。
遺伝子発現解析からも、脳Tregは他の組織Tregに類似していることが示されました。しかし脳Tergには、それらにない特徴的な遺伝子発現もみられました。特に通常Tリンパ球にみられない神経関連遺伝子がいくつか発現しています。我々は脳TregはcAMPを上昇させるセロトニン受容体7(Htr7)(注4)を発現していることに注目しました(図5a)。cAMPはTregの増殖を促進すると同時に機能を増強させることが知られています。予想通り単離された脳TregはHtr7依存的に増殖・活性化されました。脳梗塞慢性期にセロトニンを投与すると脳Tregが増加し神経症状が改善しました(図5b)。また選択的セロトニン再取り込み阻害薬(SSRI)にも同様の効果がありました。SSRIはうつ病治療薬として使われる、脳内セロトニンの濃度を上昇させる薬です。脳梗塞慢性期の神経症状の改善にも効果があるとする報告もいくつかあります(文献3)。SSRIの効果の一部は脳Tregを介している可能性があります。よって脳Tregは脳という特殊な環境に順応した機能を獲得しており、神経伝達物質によって刺激を受けて増幅するという非常に興味深い性質を持っています。どのような機構で脳Tregは神経関連遺伝子を発現するのかは、解明すべき今後の重要な課題です。
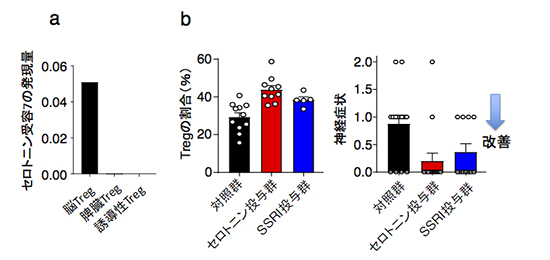
図5.
脳Tregにおける7型セロトニン受容体(Htr7)の発現(a)。セロトニン(5-HT)もしくはセロトニン再取り込み阻害剤(SSRI)は脳Tregを増加させ神経症状を改善する(b)。
脳Tregによるアストログリオーシスの制御機構
ではどのような仕組みで脳Tregは脳機能改善に寄与しているのでしょうか?脳内Tregを除去、あるいは減少させるとアストロサイトの過剰な活性化(注3)が認められ、運動野の神経細胞がアポトーシス(細胞死)を起こしていました。これがTreg除去による運動機能回復の遅れに繋がっていると考えられます。アストロサイトの活性化は、瘢痕形成を誘導し神経細胞を炎症から隔離するために必要ですが、過剰に活性化されたアストロサイトは神経毒性因子を産生し、むしろ神経細胞を傷害したり、神経伸長を阻害したりします(文献4)。脳Tregはアストロサイトの過剰な活性化(アストログリオーシス)を抑制していることが分かりました。アストロサイトの活性化にはIL−6などの炎症性サイトカインが重要です。試験管内で脳Tregと活性化したミクログリアやアストロサイトを共培養すると、IL−6の産生が抑制されることが分かりました(図6上)。またTregの移入により、アストロサイトの過剰な活性化が抑制されると同時に、IL−6の下流で活性化されるSTAT3のリン酸化が抑制され、神経症状が改善しました。脳Tregの特徴のひとつはアンフィレグリン(Areg)を強く産生することですが、Aregの脳内投与により、アストロサイトの活性化が抑制され、神経症状が改善しました。試験管内の実験で抗Areg抗体を投与すると、脳TregによるミクログリアやアストロサイトからのIL−6産生抑制が部分的に解除されました(図6上)。さらに個体でもAregを欠損するTregでは野生型Tregで認められたアストロサイトの抑制や神経症状の改善が認められませんでした(図6下)。AregがIL-6産生を阻害する分子機構は不明であるものの、Aregは脳Tregの重要な機能分子といえます。またAregは神経幹細胞の増殖に直接的に働いている可能性もあります。
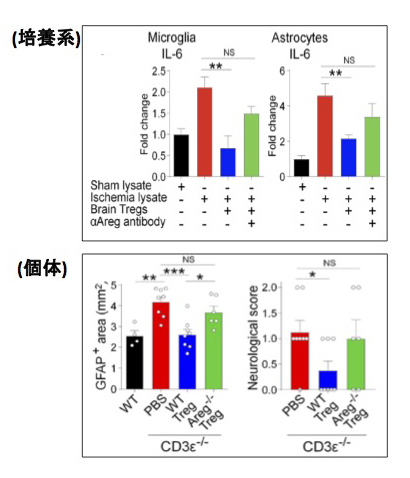
図6.
Tregはアンフィレグリン(Areg)に依存的にIL-6の産生を抑制(上)し、脳梗塞後のアストログリオーシスを抑制し神経症
状も改善する(下)。
ヒトへの応用と今後の展望
本研究のまとめを図7に提示します。脳Tregは何らか脳内自己抗原を認識し増幅し、ケモカインによって脳内に誘引されて、IL-2やIL-33、セロトニンの作用で増幅します。脳TregはAregなどの神経保護因子を放出し、アストロサイトの過剰な活性化を抑制することで脳梗塞による神経症状を緩和します。実際にヒト脳内にTregが集積しているのかどうかは不明ですが、剖検では脳梗塞部位にT細胞の集積がみられます。またヒト脳梗塞において末梢血のTregの数と予後の関係が報告されています。実験的脳梗塞モデルで全身性にTregを移入し治療効果を示した研究もありますが、我々の検討では慢性期のTregの移入では脳への浸潤の増加はほとんど認められませんでした(伊藤ら未発表)。脳Tregの末梢からの浸潤にはある程度の数的制限があることが考えられます。将来的には間葉系幹細胞で行われているように自家Tregを脳内に直接投与する方法も検討されるべきでしょう。
脳内炎症は、脳梗塞だけではなく脊髄損傷などの脳脊髄組織の損傷以外にも、多発性硬化症のような自己免疫疾患やアルツハイマー病やパーキンソン病のような神経変性疾患でも起こることが知られています。先に述べたようにセロトニントランスポーター阻害剤(SSRI)は脳梗塞による神経症状を改善することが複数報告されています。また多発性硬化症患者のTregがセロトニン刺激によって増殖することも報告されています。これらの脳内炎症にも獲得免疫が発動され脳Tregが浸潤、集積し、神経症状に重要な役割を果たしている可能性が示唆されます。
組織損傷後の炎症の慢性期にTregが修復に働いているのは脳だけではありません。多くの組織で一見炎症が治まったように思えてもTregが組織修復や恒常性の維持に働いている可能性があります。組織におけるTregの生存や増殖をもたらす自己抗原やTregを刺激するリガンドは、組織特異的なTregの機能に重要である可能性が高いと考えられます。自己抗原やリガンドの探索も含め、Tregの組織特異的なフェノタイプを解析することによって、組織特異的なTregを誘導、増殖することができれば、他の臓器の組織損傷においてもTregを用いた組織特異的な治療法の開発につながることが期待されます。
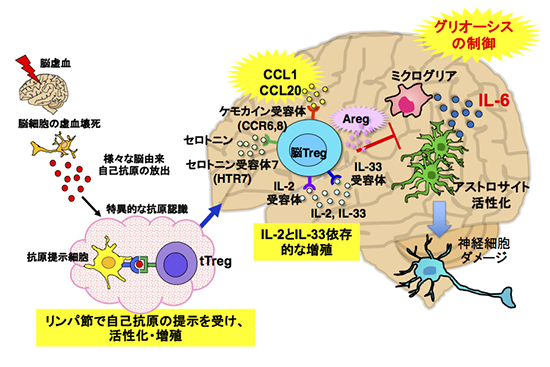
図7. 脳Tregの活性化、集積、増幅および機能
見た目には炎症は際立たないが、慢性期はTregを中心に炎症の平衡状態にある。
【用語解説】
(注1) 制御性T細胞(Treg)
T細胞の一種。主に胸腺や消化管で発生し、普段は自己に対する免疫応答を抑制している。炎症を抑え、アレルゲン、食物や胎児に対して免疫を発動させない機能も有するが、がん(腫瘍)に対しては腫瘍免疫を抑制しその成長を促進してしまう。
(注2) 脳梗塞モデルマウス
脳血管を閉塞させ人為的に脳梗塞をおこしたマウス。本研究では、細い塞栓糸を頚動脈から挿入して脳血管(中大脳動脈)に到達させ閉塞させる手技を用いた。
(注3) アストロサイト
脳内に存在するグリア細胞の1つで通常は神経の支持細胞であるが炎症によって活性化されて神経傷害に働くこともある。このような状態をアストログリオーシスという。
(注4) セロトニン受容体
セロトニンは脳内で働く神経伝達物質のひとつで、様々な脳の機能や精神の安定に深く関わっている。セロトニンの受容体は7種類以上知られており、それぞれが異なった作用を持つ。
参考文献
Brain regulatory T cells suppress astrogliosis and potentiate neurological recovery.
Ito M, Komai K, Mise-Omata S, Iizuka-Koga M, Noguchi Y, Kondo T, Sakai R, Matsuo K, Nakayama T, Yoshie O, Nakatsukasa H, Chikuma S, Shichita T, Yoshimura A.
Nature. 2019 Jan;565(7738):246-250. doi: 10.1038/s41586-018-0824-5. Epub 2019 Jan 2.
【本研究に先行する参考文献】
- Tissue Tregs.
Panduro M, Benoist C, Mathis D.
Annu Rev Immunol. 2016 May 20;34:609-633. - Fluoxetine for motor recovery after acute ischaemic stroke (FLAME): a randomised placebo-controlled trial.
Chollet F, Tardy J, Albucher JF, Thalamas C, Berard E, Lamy C, Bejot Y, Deltour S, Jaillard A, Niclot P, Guillon B, Moulin T, Marque P, Pariente J, Arnaud C, Loubinoux I.
Lancet Neurol. 2011 Feb;10(2):123-130. - Neurotoxic reactive astrocytes are induced by activated microglia.
Liddelow SA, Guttenplan KA, Clarke LE, Bennett FC, Bohlen CJ, Schirmer L, Bennett ML, Münch AE, Chung WS, Peterson TC, Wilton DK, Frouin A, Napier BA, Panicker N, Kumar M, Buckwalter MS, Rowitch DH, Dawson VL, Dawson TM, Stevens B, Barres BA.
Nature. 2017 Jan 26;541(7638):481-487.

左:吉村昭彦(微生物学・免疫学教室教授)、右:伊藤美菜子(同特任助教)

