慶應発サイエンス
iPS細胞を用いた胎児の形態異常の解明
研究の背景
胎児の時期に症状が出現しはじめ、生まれつき障害を持つ症候群では、これまで病気ができあがる過程を観察することができず、どのようにして症状が形成されているかを解明することが困難でした。動物を用いて病気モデルを作り、病気を研究する試みもなされていますが、動物とヒトとの違いのため期待した病気モデルとならなかったり、モデルとなる動物が犠牲になるという倫理的な課題がありました。
人工多能性幹細胞(iPS細胞)は、少量の患者の皮膚や血液より作成することができ、また身体のあらゆる組織や細胞になることが可能な細胞株です。iPS細胞を利用して、病気の主体となっている組織の細胞種を作り出すことにより、これまで観察することが困難であったヒト胎生期の細胞を作り出し、観察したり解析することが可能となりました。
研究の概要
我々は、生まれつき目、耳や顔面形成に異常を持つCHARGE症候群患者について、iPS細胞を用いた病気モデルを作成しました。頭部神経堤細胞は、胎児の間に目、耳、鼻などの感覚器や顔の形成などに重要な役割を持つために、CHARGE症候群では、神経堤細胞が病気の形成に大きく関係していると長らく推測されてはいましたが、明らかにはされていません。2004年にCHARGE症候群の患者さんにCHD7遺伝子異常があることが分かり、この遺伝子が、ヒトでどのような働きをしているのか注目が集まっています。
我々は、CHARGE症候群の患者さん2名およびそれぞれの親御さんより協力を得て5mm大の皮膚細胞を採取し、それよりiPS細胞を作りました。作製したiPS細胞を、培地(細胞を培養するための液体)などの細胞環境を調整することで神経堤細胞を作製しました。この神経堤細胞はさらに神経や骨、軟骨、筋肉、脂肪などの様々な組織になることができます。またCHARGE症候群ではない健常者の皮膚細胞からもiPS細胞を作製し、同様に神経堤細胞を作りました。神経堤細胞は胎児の間に作られ、自ら動いて、身体の色々な場所の組織に行くことが知られています。この細胞の動きを観察した結果、CHARGE症候群患者より作製された神経堤細胞は周りの細胞とお互いに引っ付いたままであり動き出さず(図1)、また動き出した後もその速度が遅いことが分かりました(図2)。

図1. 健常者とCHARGE症候群患者のiPS細胞由来神経堤細胞の比較
CHARGE症候群患者iPS細胞由来神経堤細胞はお互いに接着した状態が持続し、個々にバラバラとなりにくい。
(参考文献のFig4 (A)より)
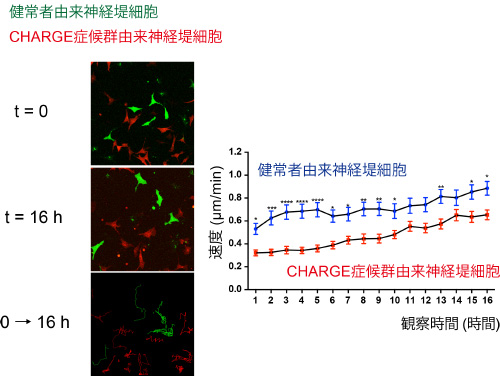
図2. 培養皿上での健常者とCHARGE症候群患者のiPS細胞由来神経堤細胞の動く速度の違い
健常者およびCHARGE症候群患者iPS細胞由来神経堤細胞を別々の色に染めて同じ環境下で16時間動きを観察したところ、CHARGE症候群細胞株で速度が低下していた。
(左:参考文献のFig6 (A)(一部改変)、右: Fig6 (B)より)
次に、この動きの障害(遊走障害)が実際に胎児内でも起こっているか否かを調べるために、作製した神経堤細胞をニワトリ胚に移植したところCHARGE症候群患者由来の神経堤細胞では遊走障害が起こることが判明しました(図3)。
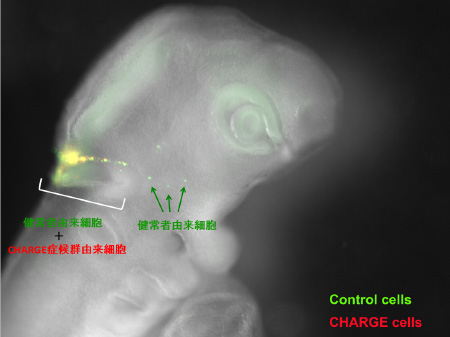
図3. ニワトリ胚内での健常者とCHARGE症候群患者のiPS細胞由来神経堤細胞の動く速度の違い
健常者由来神経堤細胞(緑)とCHARGE症候群由来神経堤細胞(赤)を別々に染めたものをニワトリ胚の背中側に移植し36時間後に観察した。健常者由来細胞の方が腹側に多く到達していた(黄色は健常者由来とCHARGE症候群由来細胞が重なってみえた部位)。
実際に患者の神経堤細胞を観察しても、遊走に障害があることが、今回の研究により初めて明らかになりました。近年、様々な疾患の研究において、iPS細胞を利用した病気のモデル作製が行われていますが、それらはRNA やタンパク発現を解析して病態を類推するものが主流になっています。今回、我々はRNAやタンパク発現だけではなく、実際に細胞の動きを培養皿上およびニワトリ胚の中で観察することにより、遊走障害を直接的に観察するモデルの作成に成功したことがこの研究の成果でもあります。
研究の成果と意義・今後の展開
今までの研究により、CHARGE症候群はCHD7という遺伝子の機能不全が原因となっており、いろいろな遺伝子の発現を制御していることが知られています。我々が今回作成したiPS細胞モデルを用いることで、神経堤細胞の遊走障害に直接関わる因子を見つけ出し、それを解明していくことが可能になりました。このiPS細胞を用いた病気モデルは、細胞の動きを実際に観察することができるというユニークなシステムであり、より直接的に障害の形成を観察できる点で優れています。このモデルを応用し、神経堤細胞の障害により生じる多くの病気のモデル系を探索することで、病態解明および治療を目標とした研究への道筋につながることを期待しています。安全性が重要視される様々な創薬研究において、このモデルは初期の胎児の神経堤細胞に影響を与える薬剤の安全性スクリーニングにも応用可能です。今までは動物実験を用いて新規開発された薬剤の安全確認が行われていますが、ヒトとの種差が存在するために、動物実験では問題がなかった薬剤がヒトには毒性を与えたという事例もあります。本研究で用いた細胞はヒト細胞であり、ヒトへの影響を直接的に確認することができるというだけでなく、動物実験の負担を軽くし、より少ない動物実験で薬の安全性確認をすることが可能になるのはないかと考えています。
参考文献
CHARGE syndrome modeling using patient-iPSCs reveals defective migration of neural crest cells harboring CHD7 mutations.
Okuno H, Renault Mihara F, Ohta S, Fukuda K, Kurosawa K, Akamatsu W, Sanosaka T, Kohyama J, Hayashi K, Nakajima K, Takahashi T, Wysocka J, Kosaki K, Okano H.
eLife. 2017 Nov 28;6. pii: e21114. doi: 10.7554/eLife.21114.

左:筆者(生理学教室助教)、右:岡野栄之(同教授)

