慶應発サイエンス
内耳性難聴に対するiPS創薬研究-新規病態の発見と治療薬の同定-
内耳は細胞診もできず、画像検査でも限られた情報しか得られない
老人性難聴や突発性難聴、メニエール病などに代表される難聴の多くは内耳に原因があることが知られており、65才以上の人口の30~40%が難聴によりハンディキャップを有しています(WHO による報告)。また、先天性疾患の中でも難聴はもっとも頻度が高く(新生児500~1,000人に1人)、その約半数は遺伝性難聴です。
一般に、疾患の理解には、病気の細胞を直接採取(生検)して観察したり、あるいは病気が進行している最中の組織を調べたりする(病理組織診)ことがとても大切です。ところが、内耳は骨の内部にあるリンパ液に満たされた臓器で検査のために細胞を採取することはできません。大きな変化はCTや MRIで捉えられますが、内耳は身体の中で最も小さい臓器であり、多くの場合画像検査でも何も見つかりません。疾患の原因が十分に突き止められないと、原因に対する新しい治療法の開発もどうしても遅れてしまいます。
iPS技術を用いた難聴患者の内耳細胞の作製
京都大学の山中伸弥教授らによって世界で初めて作製されたiPS細胞は、身体を構成するすべての組織や臓器に分化できる能力(多能性)を持つため、原理的に身体中のあらゆる細胞を試験管内で人工的に作製することが可能です。そこで、世界中の多くの研究者がこの技術を利用して患者さんの病気の細胞を作製し、顕微鏡で観察するアプローチを採用しています(疾患iPS細胞研究)。研究チームは、患者さんから直接得ることができない病気の内耳の細胞を、このiPS細胞の技術を用いて作製することにしました。
まず、ヒトiPS細胞から内耳細胞を効率的に安定して作成する方法を開発し、内耳の中でも聴覚を担当する「蝸牛」のほぼ全ての種類の細胞をiPS細胞から作製する方法を見出しました。この方法を用いれば、目の前にいる人の蝸牛の細胞を大量に用意して研究に活かすことができます。
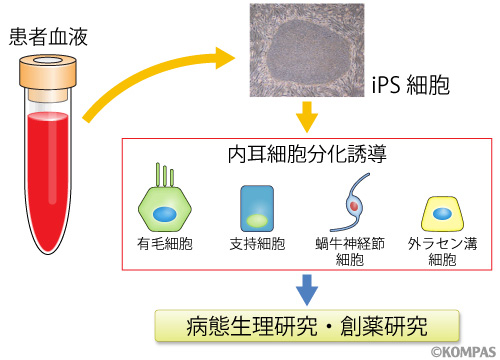
図1.ヒトiPS細胞による内耳細胞の作製
遺伝性進行性難聴Pendred症候群の内耳細胞は、異常タンパクの細胞内凝集を伴う
難聴には色々な種類があり、たとえば加齢や環境因子なども聴力に影響を与えます。そこで私たちは、両側進行性の遺伝性難聴の中で、原因遺伝子は特定されているが難聴発症の詳細なメカニズムが知られていないものに着目しました。歴史を紐解くと、多くの未知の疾患においてその発症メカニズムが遺伝性発症家系の研究から明らかにされてきたからです。
Pendred症候群は遺伝性難聴の中で2番目に患者数の多い病気で、SLC26A4遺伝子の変異によるペンドリン(PENDRIN)タンパクの異常が原因であることが知られています。本疾患の患者さんは進行性の難聴を起こしますが、この病気のヒト型遺伝子変異マウスは進行性難聴を再現できず、なぜ難聴が進行していくのかをうまく説明することはできませんでした。このため、治療法の開発は難しいと考えられていました。
研究チームでは、Pendred症候群患者さんの血液から疾患特異的iPS細胞を作製し、この患者iPS細胞と健常者iPS細胞からそれぞれ内耳細胞を作製して、比較検討しました。その結果、患者iPS細胞から作られた内耳細胞においてのみ細胞内に異常なペンドリンが蓄積し(図2)、パーキンソン病やアルツハイマー病などの進行性の中枢神経障害を呈する神経変性疾患にみられるような凝集体が形成されることがわかりました。Pendred症候群患者由来のこの内耳細胞は細胞ストレスに非常に弱く、細胞がより死にやすくなっていることがわかりました(細胞脆弱性)。
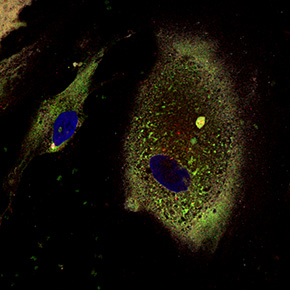
©慶應義塾大学・NHO東京医療センター
図2.患者iPS細胞から作製した内耳細胞(ペンドリンが蓄積している)
オートファジー促進薬が内耳細胞の細胞死を保護することを発見
続いて、Pendred症候群の難聴の進行の治療薬を開発するため、研究チームは複数の薬剤の中から、この細胞ストレスに対する細胞脆弱性を改善する薬剤を探しました。その結果、抗糖尿病薬であるメトホルミンと、免疫抑制剤であるラパマイシン(シロリムス)が脆弱性を改善することを発見しました。
これら2剤は全く異なる疾患で使われている既存薬ですが、どちらもオートファジー促進作用があることが知られています。そこでこれらの薬剤を使用するときに、同時にオートファジーの最後のステップを阻害する薬剤を添加したところ、細胞死保護作用がなくなることがわかりました。オートファジーの促進が、Pendred症候群の内耳細胞の細胞死を抑える働きがあることが示されたわけです。
研究の意義と今後の課題
本研究によって、Pendred症候群の進行性難聴は、多くの神経変性疾患と同様のメカニズムによって進んでいくことが明らかにされました(「内耳変性仮説」)。これは、マウスモデルの実験ではわからなかった研究成果であり、ヒト患者細胞を直接扱えるiPS細胞研究ならではの成果です。また、本研究によってオートファジー促進剤が進行性難聴を抑制する治療薬となる可能性が示唆されました。
今回使用した、ヒトiPS細胞から内耳細胞を作製する方法を用いることで、ヒト型遺伝子変異マウス作製で疾患モデルを作ることができなかった他の難聴に対しても研究を進められる可能性があります。今後はこのアプローチによって、他の遺伝性難聴疾患の病態解明や、新しい治療法の開発が期待されます。
両側特発性難聴などの内耳に原因のある進行性難聴には、遺伝子変異のほかにも多くのメカニズムが仮説として考えられていますが、ヒトの内耳の細胞は採取できないため、臨床現場では最後まで原因が明らかにならないことがしばしばあります。研究チームはこれらの原因不明の進行性難聴の中に「内耳変性」を起こしている患者さんが含まれている可能性を視野に入れており、今後このヒトiPS技術を用いたアプローチで徐々に明らかにしていこうと考えています。
参考文献
Cochlear Cell Modeling Using Disease-Specific iPSCs Unveils a Degenerative Phenotype and Suggests Treatments for Congenital Progressive Hearing Loss.
Hosoya M, Fujioka M, Sone T, Okamoto S, Akamatsu W, Ukai H, Ueda HR, Ogawa K, Matsunaga T, Okano H.
Cell Rep. 2017 Jan 3;18(1):68-81. doi: 10.1016/j.celrep.2016.12.020.

左:藤岡正人、右:細谷 誠
稿を終えるにあたり、本研究に対し長年のご指導をいただきました慶應義塾大学医学部生理学教室 岡野栄之教授、赤松和土准教授(現 順天堂大学医学部教授)、NHO東京医療センター臨床研究センター聴覚・平衡覚研究部 松永達雄部長、慶應義塾大学医学部 耳鼻咽喉科学教室 小川郁教授に深謝いたします。

左から、耳鼻咽喉科学教室 小川郁教授、生理学教室 岡野栄之教授

