慶應発サイエンス
間葉系幹細胞の免疫性線維化における役割
はじめに
全身の線維化は、自己免疫疾患が持つ特徴の1つで、免疫系(注1)が自己の細胞を異物と誤って認識し、体の結合組織を攻撃することによって生じます。T細胞をはじめとした免疫担当細胞が結合組織に集積して、特に強皮症(注2)では皮膚硬化をきたします。そして、肺や他の内臓の臓器に障害を与えることもあります。しかしこれまで、何が個体の結合組織にT細胞を集積させるのか不明な部分がありました。
免疫系はまず、細胞表面蛋白を自己と認識します。これには主要組織適合抗原と呼ばれる一群の細胞表面膜蛋白が主要な役割を果たしていますが、細胞表面膜蛋白にはこの他にもマイナー組織適合抗原(注3)と呼ばれる別の蛋白も存在します。これまで、造血幹細胞移植後の合併症のひとつであり、自己免疫疾患に類似する慢性移植片対宿主病(GVHD:graft-versus-host disease)(注4)の病態は、ドナーの造血幹細胞から分化したT細胞やマクロファージによって引き起こされると考えられてきました。
骨髄幹細胞には造血幹細胞(hematopoietic stem cell. 以下、HSC)(注5)と間葉系幹細胞(mesenchymal stem cell. 以下、MSC)(注6)がありますが、本研究では、ドナーのHSCではなくドナーのMSCが、移植後にレシピエントのT細胞を自分の細胞に対して誤って反応するように変化させ、自己免疫疾患様の病態を引き起こすことをつきとめました。
研究の概要
今回用いた自己免疫疾患に類似する慢性GVHDモデルマウスでは、ドナー(B10.D2マウス)とレシピエント(BALB/cマウス)の細胞同士について、主要組織適合抗原は一致していますが、マイナー組織適合抗原が不一致であるマウスの組み合わせを用います。その結果、ドナー骨髄幹細胞がレシピエント体内で過剰な免疫応答を引き起こし、ヒトの慢性GVHDに極めて類似した所見を呈します。
このモデルマウスで自己免疫疾患の線維化がどのように発症するか病態を追究するために、ドナー骨髄幹細胞の中から新鮮HSCと新鮮MSCを分離して、培養をせずにレシピエントへ移植して多方面から検証しました。MSCがレシピエントにおいて、異常な免疫応答を引き起こすか否か、全身線維化に関わるか否かを追究しました。
筆者らは、このような自己免疫疾患(注7)に類似した慢性GVHDモデルマウスを用いて、造血幹細胞移植後の合併症のひとつである慢性GVHDや自己免疫疾患によって生じる強皮症などの線維化疾患(注8)の病態を引き起こす細胞源が、骨髄に存在するMSCであることを発見しました。
免疫性線維化におけるMSCのはたらき
MSCが線維化病態の中心的役割を果たす線維芽細胞の細胞源であることを特定
マウスMSCとHSCを培養せずに直接分離し、強皮症モデルマウスに骨髄幹細胞をさまざまな組み合わせで移植し、その動態を調べました(図1)。その結果、主要組織適合抗原が一致し、マイナー組織適合抗原が不一致であるドナーの新鮮MSCを移植した時のみにレシピエントにおいてGVHDに類似した炎症および線維化を起こすことを各臓器で示しました。
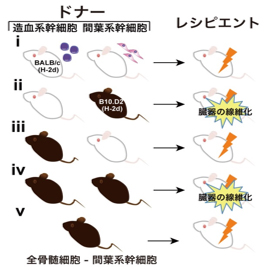
図1.骨髄幹細胞の様々な組み合わせによる移植が及ぼす臓器の線維化の検証
(参考文献より転載)
- レシピエント(白マウス)から造血幹細胞(HSC)と間葉系幹細胞(MSC)の移植。臓器線維化(-)。
- レシピエントHSCとドナー(黒マウス)のMSCの移植。強皮症に似した臓器線維化(+)。
- ドナーHSCとレシピエントMSCによる移植。臓器線維化(-)。
- ドナーHSCとドナーMSCによる移植。強皮症に類似の臓器線維化(+)。
- ドナーMSCを除去して移植。臓器線維化(-)。
ドナーMSCの標的臓器への移動
蛍光色素(GFP)で緑色に標識されたドナーマウスのMSCを移植したのち、レシピエントの標的組織におけるドナーMSC由来線維芽細胞の集積を確認しました。また、自己免疫疾患の標的臓器の1つである涙腺の培養線維芽細胞にも、ドナー由来MSCを多数確認しました。さらに、T細胞とドナーMSCの相互作用の局在を示しました。
ドナーMSCとの相互作用によってレシピエントT細胞は自己の細胞を異物として認識
ドナーMSC移植後のレシピエントT細胞を、胸腺がないためにT細胞が作られない突然変異系統のマウスであるヌードマウスにAdoptive transfer(注9: 養子移入)をしたところ、強皮症様慢性GVHDによる炎症と線維化が引き起こされました。これによって、T細胞が自己免疫疾患を引き起こすタイプに変化したことが判明しました。
ドナーMSC移植により末梢血中血清IL-6産生が増加し末梢血制御性T細胞が減少しIL-17産生Th17細胞の増加が認められ自己免疫疾患類似の所見が生じていることが確認されました(図2)。
MSC除去により標的臓器線維化を抑制
骨髄幹細胞からドナーMSCを除去して移植した結果(図1,v)、涙腺、結膜、肺、肝臓、皮膚などでの標的臓器での線維化病変が抑制されることが確認されました。
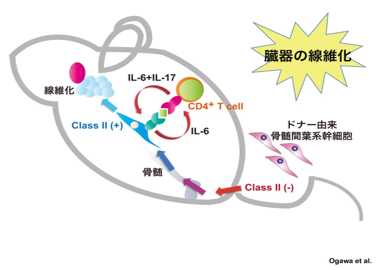
図2
ドナーMSC移植によりドナーMSCがレシピエントT細胞と反応して末梢血中血清IL-6産生が増加し末梢血の制御性T細胞が減少しIL-17産生Th17細胞の増加を認める。ドナーMSCは病態の発症進行に一致してMHC class II(主要組織適合抗原クラスII)を発現することを確認した。
研究の意義および今後の展開
本研究成果は、自己免疫疾患による肺線維症、肝硬変、強皮症などの線維化疾患の病態解明と新規治療法の開発へ道を開く可能性を秘めています。本研究の成果によって、線維化をきたすさまざまな自己免疫疾患の病態解明と新規治療法の開発につながるとともに、GVHDの予防法を開発できる可能性も考えられます。
さらには、骨髄移植は、血液悪性疾患に対する根治療法として広く行われていますが、骨髄移植の重篤な合併症であるGVHDの予防法は無く、治療に対する大きなリスクとなっています。骨髄移植の治療成績の向上に結びつく手がかりともなると考えられ、医学的な意義は大きいと考えます。
【用語解説】
(注1)免疫系
免疫をつかさどるシステムのことで、人体の自己にとっての異物を非自己と認識し排除するシステムです。免疫担当細胞とリンパ器官をはじめとする複雑なネットワークから構成されています。免疫担当細胞から作られる抗体や、サイトカインも免疫系の大切な構成因子です。免疫細胞は骨髄中の造血幹細胞から分化し、骨髄系前駆細胞およびリンパ系前駆細胞に分化します。間葉系幹細胞も免疫系を強めるものと弱めるものがあるとされています。
(注2)強皮症
線維化と血管内皮障害を特徴とする、原因不明の自己免疫疾患です。自己免疫異常が病態形成に関与していると推察されています。
(注3)マイナー組織適合抗原
組織適合抗原の1つです。T細胞に抗原を提示するための膜蛋白のうち主要組織適合抗原以外のもので、多くは免疫系とは無関係の分子に由来します。遺伝子の突然変異に起因するとされています。これらの分子が細胞内で酵素分解されそのペプチドが細胞膜表面のMHCに結合して細胞表面に結合するとされています。
(注4)移植片対宿主病(Graft-versus-host disease: GVHD)
血液悪性疾患等の根治療法としての造血幹細胞移植の後に生じる、晩期合併症のうちの1つ。GVHDとはドナー(造血幹細胞提供者)の移植片とレシピエント(移植希望者)の細胞、または組織との間に生じる免疫応答で、眼、口腔、肺、皮膚、腸管、肝臓が標的臓器となります。
(注5)造血幹細胞(HSC)
すべての血液細胞を作りだすことができる分化能と自己複製能を持つ未分化細胞。間葉系幹細胞とともに骨髄幹細胞のうちの1つ。造血幹細胞からの分化によりT 細胞、B細胞などのリンパ系細胞と赤血球、顆粒球、巨核球などの骨髄系細胞に分かれます。
(注6)間葉系幹細胞(MSC)
間葉系幹細胞は、間葉系に属する骨、軟骨、脂肪細胞への分化能と自己複製能を持つ未分化細胞です。間葉系幹細胞は皮膚や脂肪にも存在することが示されていて、由来組織により特性が異なります。骨髄間質細胞が分化誘導されることにより、間葉系に属する細胞(骨細胞、軟骨細胞、脂肪細胞など)への分化能を持っています。
(注7)自己免疫疾患
何らかの遺伝的、環境因子により、免疫担当細胞が自己の組織を誤って認識し過剰な免疫応答が自分の組織を障害することによって生じる疾患です。強皮症、全身性エリテマトーデス、関節リウマチ、外分泌腺が特に障害されるシェーグレン症候群、などがあります。本研究で用いたモデルマウスでは、マウスの骨髄幹細胞を移植することで、自己免疫疾患である強皮症(注2)のような臓器線維化を主体とした病態を発症することが知られています。
(注8)線維化疾患
線維化は、体を支える組織を構成する結合組織が過剰に増殖する現象です。免疫担当細胞や線維芽細胞の活性化、増殖により結合組織に過剰な膠原線維と細胞外器質の沈着が生じ組織が固くなって臓器の機能不全が生じます。線維化疾患には肝硬変、腎硬化症、肺線維症などがあります。現在、線維化に対する良い治療法がなく、新しい治療法が望まれています。
(注9)Adoptive transfer(養子移入)
ある特定の生理機能を持つ細胞集団を、その機能を欠いている個体に移植して、長期的に機能を獲得させること。ある抗原に刺激されて免疫状態にある個体から得られたリンパ球を未感作個体へ移植することによって後者を免疫状態に導くことが例に挙げられます。
参考文献
MHC-compatible bone marrow stromal/stem cells trigger fibrosis by activating host T cells in a scleroderma mouse model.
Ogawa Y, Morikawa S, Okano H, Mabuchi Y, Suzuki S, Yaguchi T, Sato Y, Mukai S, Yaguchi S, Inaba T, Okamoto S, Kawakami Y, Tsubota K, Matsuzaki Y, Shimmura S.
eLife. 2016 Jan 26;5:e09394. doi: http://dx.doi.org/10.7554/eLife.09394

左:小川葉子、右:森川 暁
稿を終えるにあたり、本研究に対し長年のご指導をいただきました慶應義塾大学医学部生理学教室 岡野栄之教授、松崎有未准教授(現 島根大学医学部教授)、慶應義塾大学医学部 眼科学教室 榛村重人准教授、坪田一男教授に深謝いたします。

左から、松崎有未先生、岡野栄之先生、坪田一男先生、榛村重人先生

