慶應発サイエンス
筋ジストロフィーに対する筋肉再生療法の開発
はじめに
成人の骨格筋には『筋衛星細胞』と呼ばれる幹細胞が筋線維の周囲に僅かながら存在します(図1)。通常は、筋衛星細胞は睡眠状態にあり何もしていません。しかし、運動や筋傷害時には、筋肉の損傷に応じて筋衛星細胞が活性化・増殖して骨格筋の再生に至り、筋力が回復することが知られています。筋肉細胞には骨格筋のほか、心臓の収縮を行う心筋、血管の収縮などに関わる平滑筋などが存在しますが、この筋衛星細胞によって再生するのは骨格筋のみです。
デュシェンヌ型筋ジストロフィーは、骨格筋細胞の形を維持するために重要な働きをしているジストロフィン遺伝子の変異によって筋肉細胞が壊れやすくなる病気と考えられています。デュシェンヌ型筋ジストロフィー患者さんにおいても、骨格筋に幹細胞が存在するために、病気の初期は筋衛星細胞が活発に増殖して筋損傷に対応していますが、罹病期間が長くなると筋衛星細胞が疲弊して活性化・増殖できなくなり、骨格筋の再生能力が低下してしまうと考えられています。このような筋ジストロフィーに対して骨格筋の再生を強くそして長期に渡り促すことができれば、筋力低下を免れることができるのではないかと考えられますが、動物実験でも大きな効果は得られていませんでした。
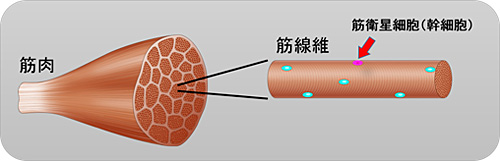
図1. 骨格筋と筋線維
いわゆる筋肉とは、たくさんの骨格筋細胞が集まった組織をさします。筋線維における青丸は筋肉細胞の核です。筋衛星細胞は小型の細胞で、筋線維周囲に僅かに存在しています。
G-CSF受容体の活性化筋衛星細胞における発現
筋衛星細胞は、骨格筋傷害に反応して活性化筋衛星細胞となり、増殖・分化し骨格筋前駆細胞(筋芽細胞)を経て成熟骨格筋となる。我々は以前、子供のマウスにおいて骨格筋前駆細胞で顆粒球コロニー刺激因子(Granulocyte-colony stimulating factor: G-CSF)受容体が発現していること、さらに大人のマウスにおいても筋損傷後の骨格筋前駆細胞でG-CSF受容体が発現していることを発見しました。さらに急性筋損傷後にG-CSFを投与すると、筋肉の再生が促進させられることを見出していました。筋衛星細胞は骨格筋前駆細胞に比べて大きさが小さく、また数も少なく詳細な観察は難しいのですが、詳細な検討を繰り返すことにより筋衛星細胞におけるG-CSF受容体の発現様式を観察しました。筋肉の幹細胞である筋衛星細胞が活性化すると一時的に活性化筋衛星細胞の存在が観察され、活性化筋衛星細胞においてG-CSF受容体が発現することを見出しました。さらにG-CSF投与により、これらの筋衛星細胞への強い増殖作用を認めることが判明しました(図2)。
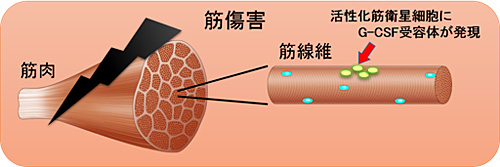
図2. 活性化筋衛星細胞にG-CSF受容体が発現
骨格筋に障害が起きると、筋衛星細胞は活性化し増殖していきます。活性化筋衛星細胞は静止期筋衛星細胞と同様に小型の細胞であり、増殖直後には集簇して観察されます。活性化筋衛星細胞においてG-CSF受容体が発現しています。
筋ジストロフィーモデルマウスにおいて十分量のG-CSFが必要である
筋ジストロフィーは骨格筋の慢性損傷疾患であり、長期に渡り骨格筋の傷害と再生を続けています。同疾患に対する骨格筋再生療法を開発するためには、筋衛星細胞に直接的に働きかけることができる強い骨格筋再生促進因子を見出す必要があります。G-CSFの筋衛星細胞に対する増殖効果より、筋ジストロフィーへの治療効果があるのではないかと考え、筋ジストロフィーモデルマウスを用いた検討を開始しました。
G-CSFが筋ジストロフィーにおいて必要かどうかを検討する為に、G-CSF受容体欠損マウスと筋ジストロフィーモデルマウスを用いた検討を行いました。G-CSF受容体欠損マウスは体中でG-CSF受容体が欠損しているマウスで、G-CSFの作用が完全になくなっています。mdxマウスはヒトデュシェンヌ型筋ジストロフィーと同様にジストロフィン遺伝子に変異があるマウスですが、軽度の筋傷害を認めるのみであり生存期間には問題ないことが知られています(図3:黄線)。またG-CSF受容体遺伝子を半分欠失させたG-CSF受容体ヘテロ欠損マウスも生存期間には影響しません(図3:赤線)。しかしながらmdx/G-CSF受容体ヘテロ欠損マウスは、筋再生が顕著に低下し致死的となることが判明しました(図3:青線)。このことから、筋ジストロフィーモデルマウスの筋再生と生存維持において、十分量のG-CSFが必要であることが判明しました。
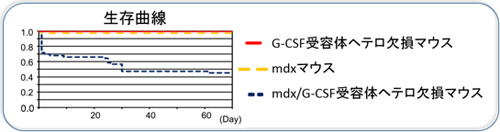
図3. モデルマウスにおける生存曲線(縦軸:生存率。横軸:産まれてからの日数)
マウスの平均寿命は約2年です。G-CSF受容体ヘテロ欠損マウスとmdxマウスにおける生存期間はほぼ正常であるといわれています。mdx/G-CSF受容体ヘテロ欠損マウスにおいては生存率が日を追うごとに低下していき生存期間の短縮が観察されました。
筋ジストロフィーモデルマウスにおいてG-CSF投与により筋肉再生は促進する
G-CSFの筋ジストロフィーへの治療効果を確認するために、より重症の筋ジストロフィーモデルマウスを用いた検討を行いました。ジストロフィン遺伝子と似た遺伝子であるユートロフィン遺伝子というものがあり、ジストロフィン遺伝子と同様に骨格筋細胞の形を維持するために重要な働きをしています。ジストロフィン・ユートロフィン二重欠損マウスは、ヒトデュシェンヌ型筋ジストロフィーに類似して、筋傷害が非常に強く致死的となります(図4:青線)。同マウスに対して3週齢からG-CSFを注射すると生存期間が著明に延長することが判明しました(図4:赤線)。さらに100日齢の同マウスは筋傷害がかなり進行した状態にありますが、同時期よりG-CSFを1週間に2回注射すると生存期間が延長することを見出しました(図4:黄線)。
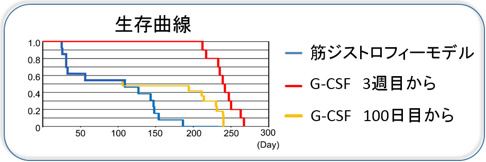
図4. モデルマウスにおける生存曲線(縦軸:生存率。横軸:産まれてからの日数)
ジストロフィン・ユートロフィン二重欠損筋ジストロフィーモデルマウスにおいては生存期間の短縮が観察されました。3週齢からG-CSFを投与することにより生存期間の延長が観察され(赤線)、また100日齢からG-CSFを投与することによっても生存期間の延長が観察されました(青線)。
おわりに
本研究においては重症の筋ジストロフィーモデルマウスへG-CSFを定期的に投与することにより、長期に渡る筋力の回復と、生存期間を著明に延長することに成功しました。今回得られた研究結果が、今後の筋ジストロフィー治療薬の開発につながるものと期待されます。
参考文献
G-CSF supports long-term muscle regeneration in mouse models of muscular dystrophy.
Hayashiji N, Yuasa S, Miyagoe-Suzuki Y, Hara M, Ito N, Hashimoto H, Kusumoto D, Seki T, Tohyama S, Kodaira M, Kunitomi A, Kashimura S, Takei M, Saito Y, Okata S, Egashira T, Endo J, Sasaoka T, Takeda S, Fukuda K.
Nat Commun. 2015 Apr 13;6:6745. doi: 10.1038/ncomms7745.
http://www.nature.com/ncomms/2015/150413/ncomms7745/abs/ncomms7745.html![]()


