慶應発サイエンス
生体内ガス分子が介するがん細胞の代謝制御機構
はじめに:生体内のガス分子
一酸化窒素(NO)や一酸化炭素(CO)、硫化水素(H2S)と聞いて、皆さんは一見毒ガスに思われるかもしれません。しかしながら私たちの体の中ではこれらガス分子が適切な場所、量が巧妙に制御されており、様々な生理機能を発揮しています。1998年にF. Murad、L. Ignarro、R. Furchgottの3氏が血管拡張の作用機序にNOが関わっていることを発見した業績でノーベル賞を受賞して以来、生体内ガス分子の重要性が広く認知されてきました。我々の研究室ではこれら生体内ガス分子がどのように産生され、正常時や病態において、どのように作用するかを解明する「ガスバイオロジー」研究を進めています。最近の研究からこれらガス分子が、がん細胞や神経細胞内の代謝制御に深く関わることが分かってきました。
がん細胞のエネルギー代謝
がん細胞は自身が増殖するために正常細胞とは異なるエネルギー利用戦略をとります(図1)。まず、通常正常細胞は酸素が十分にある環境下では、取り込んだブドウ糖をミトコンドリアにて酸化的リン酸化を通じて、エネルギー通貨であるアデノシン三リン酸(ATP)を作ります。それに対し、がん細胞は、酸素の有無にかかわらず、ブドウ糖の細胞内への取り込み量を増やすと同時に、取り込んだブドウ糖を乳酸に代謝する「解糖系」という代謝経路を活性化することでATPを得ています。この現象は発見者の名前に因み、「ワールブルグ効果」と呼ばれています。もうひとつ重要な点は、がん細胞は他の細胞種に比べ、高いストレス耐性を身につけているということです。このようながん細胞の特徴が抗がん剤による化学療法、放射線治療などのがん治療の分野で問題になっています。
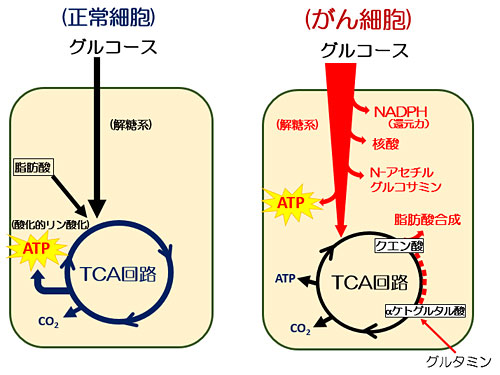
がん細胞は正常細胞とは異なりグルコースの取り込み量が多く、細胞のエネルギー通貨であるATPの産生源を主に解糖系に依存している。また、その急速な増殖能を賄うため糖質や膜脂質、核酸などの細胞構成成分が重要であるが、これらの合成系の多くは、解糖系から分岐する。それゆえ、がん細胞では様々なメカニズムにより解糖系を活性化させている。
一酸化炭素によるエネルギー代謝制御
当初、一酸化炭素はヘムの限定分解によって生じる副産物の「排ガス」としてしか考えられていませんでしたが、最近の研究からCOはNO同様に生体内においてさまざまな生理活性をもつことが分かってきました。一般にガス分子が生体内で機能を発揮する際はヘム(注1)分子上の鉄原子とガス分子が相互作用し、ヘムが結合しているタンパク質の構造を変化させることによって作用します。我々はCOの新規作用を探る過程で、必須アミノ酸であるメチオニンの代謝系にかかわる酵素の一つ、シスタチオニンβ-合成酵素(CBS)というヘム含有酵素に着目しました。メチオニン代謝ではS-アデノシルメチオニン(SAM)という代謝産物の量が制御されています。SAMは生体内のメチル基転移反応の基質分子として作用し、DNAやタンパク質のメチル化修飾(注2)を制御する上で重要です。我々による研究からCOがヘムに作用することでCBSの酵素活性を阻害し、その結果メチオニン代謝を活性化することでタンパク質のメチル化修飾をグローバルに制御することがわかりました(図2)。次に、私たちは培養がん細胞を用いて、COによってメチル化が制御されるタンパク質を調べました。その結果、細胞のエネルギー代謝に関わるタンパク質、特に、解糖系に関わる酵素群が多数メチル化修飾を受けることがわかりました。そのうち我々は、6-ホスホフルクト-2-キナーゼ/フルクトース-2,6-ビスホスファターゼ(PFKFB3)という酵素が解糖系が活性化しているがん細胞において高度にメチル化修飾を受けていることを発見しました。
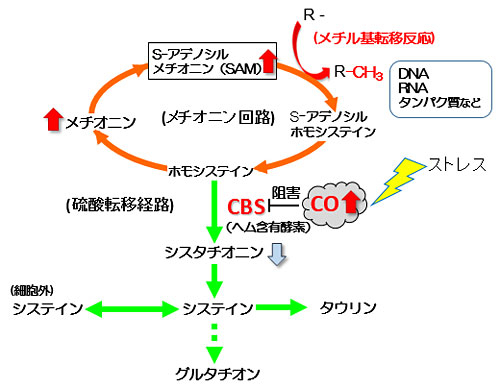
COはヘム含有タンパク質であるメチオニン代謝系の酵素、シスタチオニンβ-合成酵素(CBS)の活性を阻害する。これによりホモシステインから流れてくる硫酸転移経路を遮断する一方で、メチオニン回路中の代謝産物は増加する。この代謝経路中にあるS-アデノシルメチオニン(SAM)は細胞内のメチル基転移反応におけるメチル基供与体として働くため、COによるメチオニン回路の活性化はDNAやタンパク質など様々なメチル基転移反応を制御する。
メチル化修飾を介したがん細胞のストレス耐性獲得機構
PFKFB3はがん細胞や胚性細胞など未分化な細胞での発現量が高いことが知られており、がん細胞において解糖系を活性化する上で重要な酵素です。この酵素がメチル化されていると解糖系が活性化状態にありますが、メチル化が外れると酵素活性が低下し、不安定化することがわかりました。図3に解糖系の模式図を記します。細胞内の非メチル化型PFKFB3が増えると取り込まれたグルコースはペントースリン酸回路(注3)という代謝経路を迂回することによって、細胞増殖のために必要な核酸や、細胞内における酸化ストレスを軽減する上で重要な還元物質NADPH(注4)を多く産生することが分かりました。NADPHは細胞内のグルタチオン(注5)という解毒物質を還元化することにより、細胞が酸化ストレス耐性を維持する上で重要な働きをします。今回の実験において、PFKFB3を低メチル化状態へと人工的に誘導したがん細胞ではNADPH量および還元型グルタチオン量が増大し、抗がん剤のひとつであるシスプラチンに対して抵抗性を示すことがわかりました。
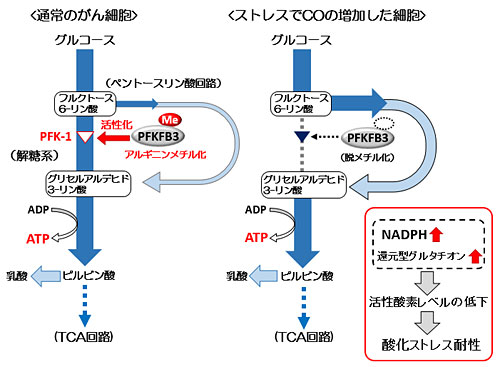
平時におけるがん細胞は、恒常的にPFKFB3がメチル化状態にあり、解糖系が活性化している。一方、様々なストレスによってがん細胞内のCO濃度が高まると、PFKFB3が低メチル化状態に陥る。その際、酵素タンパク質は不安定化し活性が低下することにより、解糖系を制御する上で重要な酵素であるホスホフルクトキナーゼ-1(PFK-1)活性が低下する。その結果、取り込まれたグルコースはペントースリン酸回路を迂回して代謝され、細胞分裂に重要な核酸や細胞内の還元力維持に重要なNADPHを生みだす。NADPHは細胞内の解毒物質であるグルタチオンを還元型に保つよう作用し、がん細胞が酸化ストレスや抗がん剤に対して抵抗性を示すようになる。
おわりに
今回、我々による研究から、がん細胞は自身が生き延びる上で重要なエネルギー産生とストレス抵抗性を同時に賄うために自身の代謝経路を切り替える術をもっていることがわかりました。その過程で解糖系酵素PFKFB3のメチル化修飾の有無が重要であり、それをCOが仲介しているという作用機序の一端を明らかにしました。今後、より詳細な本酵素のメチル化修飾メカニズムが明らかになれば、人為的にがん細胞の代謝を制御することでストレスに脆弱ながん細胞を誘導することで現在での抗がん剤治療の効果を高めることができる可能性があり、これまでのがん治療の限界を克服できる新しいがん治療法の開発につながるものと期待されます。
【用語解説】
注1) ヘム
2価の鉄原子とポルフィリンからなる金属錯体。ヘモグロビンやミオグロビンなどのタンパク質に結合する重要な非タンパク質要素。NOやCOなど生体内ガス分子はヘムの鉄原子の部分への結合能があり、そうすることでヘム含有タンパク質の機能を変化させる作用がある。
注2) メチル化修飾
DNAやRNA、タンパク質、脂質などさまざまな基質にメチル基(-CH3)が置換もしくは結合することを指す。メチル化反応はメチオニン代謝の中間代謝物質S-アデノシルメチオニン(SAM)がメチル基転移酵素によってメチル基が供与されることによって起こる。タンパク質の場合は主にアルギニン、リジン残基がメチル化修飾を受け、その機能調節に極めて重要な翻訳後修飾である。
注3) ペントースリン酸回路
解糖系から分岐する代謝経路で核酸合成の原料になる五炭糖(リボース)や還元当量であるNADPHが産生される。
注4) NADPH(ニコチンアミドアデニンジヌクレオチドリン酸)
生体内における還元的生合成に用いられる活性型電子伝達体。主に脂肪酸の合成や肝臓における解毒、グルタチオンの還元化などに使われる。
注5) グルタチオン
グルタミン酸、システイン、グリシンの3つのアミノ酸がこの順番で結合したトリペプチド。活性酸素や過酸化物などの酸化ストレスによる細胞障害に対し抗酸化作用を持つ。また体内の有害物はグルタチオンと結合し、細胞外へ排出するような解毒作用も知られている。細胞が酸化ストレスに晒されると、還元型グルタチオンの還元力で無毒化し自身は酸化されるが、グルタチオンレダクターゼによって還元型に再び変換(この際にNADPHの還元力が必要とされる)され、細胞内では常に還元型濃度を高く維持される。
参考文献
Reduced methylation of PFKFB3 in cancer cells shunts glucose towards the pentose phosphate pathway.
Yamamoto T, Takano N, Ishiwata K, Ohmura M, Nagahata Y, Matsuura Y, Kamata A, Sakamoto K, Nakanishi T, Kubo A, Hishiki T, and Suematsu M. (2014) Nature Communications Vol.5, 3480. doi:10.1038/ncomms4480
http://www.nature.com/ncomms/2014/140317/ncomms4480/full/ncomms4480.html![]()

左:筆者、右:末松 誠(医化学教室教授)

