慶應発サイエンス
がん血管のみではたらく血管増殖メカニズム
がんと血管:最先端のがん治療としての抗腫瘍血管新生療法
がんが増大するには、がん細胞に酸素・栄養を送る供給路となる血管の増殖(血管新生)が必要です。このがんの血管をたたくことで、がんの増大を止めようとする戦略は『抗腫瘍血管新生療法』と呼ばれ(図1)、がん治療における一つのオプションとして確立されつつあります。この『抗腫瘍血管新生療法』として中心的な戦略が血管内皮成長因子(Vascular endothelial growth factor; VEGF)の阻害です。VEGFは1983年にHarold Dvorakの研究グループにより発見された血管の成長に不可欠の分子です。このVEGFのはたらきを抑える中和抗体(ベバシズマブ)は2004年の米国FDA、2007年の厚生労働省の認可以降、がん治療の場で広く用いられ、大腸がん・肺がん・腎がんなど多くのがん、特に他の治療手段が奏効しない症例においても、治療効果を有することが報告され、最先端のがん治療として注目を集めています。ところが一部のがんはこのVEGF阻害薬に対して耐性(投与しているうちに効かなくなってくること)を示すとともに、VEGF阻害薬はがんの血管のみならず、がん以外の全身の血管をも傷つけてしまい、脳出血・腸管出血など、しばしば患者さんの命に係わる重大な副作用を及ぼすことが報告されています。これらを背景に、VEGFに代わる新たな『抗血管新生療法』の分子標的が世界的に探索されています。特にがんの血管と通常の血管の違いを明らかにし、がんの血管でのみ作動する分子を標的にしようという試みが世界中で活発化しています。このような背景の中わたしたちは、老化や生活習慣病(動脈硬化や糖尿病)、がんにおいて悪玉分子として忌み嫌われてきた活性酸素に目を付けました。わたしたちの長期にわたる研究の結果、活性酸素は一概に悪玉というわけはなく、実はがんの血管新生を妨げることでがんの進行を遅延させていることを見出しました。また、この活性酸素を分解するのに重要な働きを持つAtmという分子(後述)の働きを抑えることで、がんの血管新生を選択的に叩けることを見出しました。
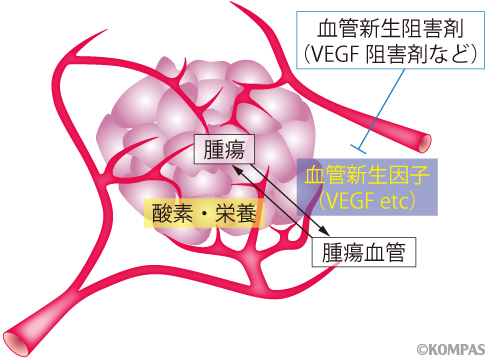
図1 がん血管と抗腫瘍血管新生療法
腫瘍細胞と血管の共同作業でがんは増大する。これをとめるのが血管新生阻害剤。
Atmによる活性酸素抑制機構はがんのみで作動する血管新生メカニズムである
Atm(Ataxia telangiectasia mutated)は、DNA損傷応答(放射線や紫外線などによりDNAにキズが付いた時に補修する機構)の中心的分子として広く知られています。その一方、Atmは活性酸素によって活性化され、細胞の活性酸素に対する自己防御機構であることも判明しつつあります。しかしながらAtmの血管新生における役割についてはこれまで全く知られていませんでした。そこでわれわれはまず、血管細胞でのAtmの活性化の程度を解析しました。その結果、健常な血管新生でAtmは殆ど活性化されませんが、がんモデルの血管新生において、活性酸素依存性に強く活性化されることを見出しました。そこでAtmを遺伝的に欠損するマウス、および血管細胞だけでAtm遺伝子を欠損するマウスを作成したところ、健常な血管には全く影響がないが、がんモデルの血管新生が殆ど起こらないことを見出しました。(図2)。なぜAtm欠損マウスではがんの血管新生が起こらないかを調べてみたところ、驚くべきことにAtm欠損マウスの血管細胞では活性酸素が異常なレベルで蓄積していました。また、このAtm欠損マウスに抗酸化剤(活性酸素を消去する薬)を投与したり、活性酸素シグナルの下流で細胞をアポトーシス(細胞の自爆システム)に向かわせるスイッチであるp38αを遺伝的に欠失させると、がんの血管新生は通常通りに起こってきました。以上の結果は、活性酸素は悪玉というよりむしろ、がんの血管新生を妨げることでがんの進行を遅延させていること、そしてAtmの働きを抑えることで、がんの血管新生を選択的に叩けることを示しています(図3)。
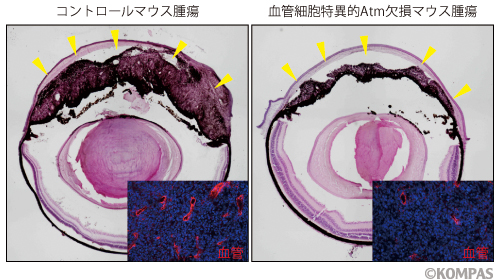
図2 がん血管におけるAtmの役割
コントロールマウス(左)に比べ、血管細胞特異的Atm欠損マウス(右)ではがん血管も減少することで、がんの増大(矢頭)が遅延する。
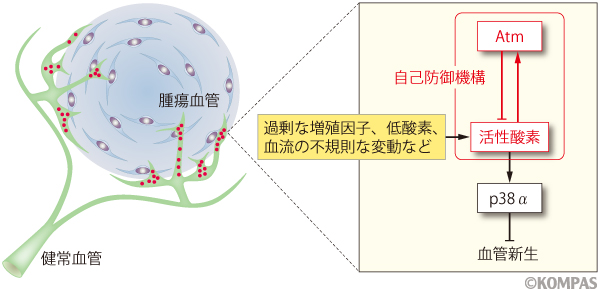
図3 Atmと活性酸素による血管新生の制御
腫瘍血管に蓄積した活性酸素はAtmによる制御を受けつつ、p38αを介し血管新生を促進する。
おわりに
活性酸素はわれわれのからだにとって有害な悪玉物質であるのは確かですが、免疫細胞における殺菌作用、細胞増殖・生存のシグナルとしての役割、さらには今回のわたしたちの研究で判明した、がん血管を抑える役割など、実は有益な側面もあることがわかっています。細胞が活性酸素の有益性を享受するためには、活性酸素の量、時間、空間全てが厳密にコントロールされている必要があります。活性酸素レベルは極めて微弱な変化であっても、生体内のあらゆる細胞の生死、活動に影響を与えます。それ故、活性酸素の上げ下げを利用した治療戦略は大いなるポテンシャルを秘め、とても有望な試みであると考えられます。その一方、正確なコントロールを失うと重大な副作用を引き起こしうる、いわゆる諸刃の剣的なじゃじゃ馬分子とも言えます。活性酸素の分子経路の詳細はまだまだ不明な点が多く、着目する細胞の種類によっても大きく異なります。これらを丁寧に解析し、包括的に理解することでがんの新たな治療戦略が拓けると考えられます。
参考文献
Pathological neoangiogenesis depends on oxidative stress regulation by ATM.
Okuno Y, Nakamura-Ishizu A, Otsu K, Suda T, Kubota Y.
Nat Med. 2012 Jul 15;18(8):1208-1216. doi: 10.1038/nm.2846.
http://www.nature.com/nm/journal/v18/n8/abs/nm.2846.html![]()

久保田 義顕(特任講師)

