慶應義塾大学が中心となりつくった日本全国の研究組織―コロナ制圧タスクフォース―
新型コロナウイルス感染症の脅威により、現在も世界中で多くの方が亡くなり、また、回復された方も後遺症に苦しんでいます。このパンデミック克服に「医学」「科学」の観点から貢献すべく、臨床家を始め、感染症医学、ウイルス学、分子遺伝学、ゲノム医学、計算科学、遺伝統計学を含む異分野の専門家が集い、ボランティアの協力も得ながら、2020年5月に慶應義塾大学の研究者が中心となって「コロナ制圧タスクフォース」を立ち上げました。コロナ対応の最前線に立つ医療従事者からも多大な協力を得た結果、発足後わずか6か月で100以上の施設が参加するネットワークが形成されました(図1)。開始から2年で6,000人以上の患者さんから血液検体と臨床データを集積することができました。新型コロナウイルス感染症のパンデミックでは患者さんの検体が手に入らないことが批判の的ともなりましたが、この全国的な組織は異例のものでもありました。
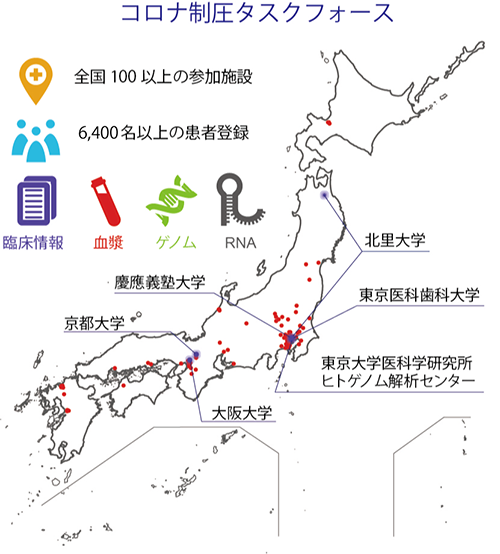
図1.全国に広がったコロナ制圧タスクフォースのネットワーク
新型コロナウイルス感染症の重症化に関わるアジア人集団に特有の遺伝子多型(バリアント)の発見
今回、コロナ制圧タスクフォースの研究チームは、新型コロナウイルス感染症に罹患して重篤化し、酸素投与やICU入室が必要となった患者さん、亡くなられた患者さんの遺伝的背景の関与を調べるために、主に第1~3波で集積した約2,400名分のDNAを用いて、遺伝子を網羅的に比較するゲノムワイド関連解析を行いました。その結果、日本人の新型コロナウイルス感染症患者では、免疫機能に重要な役割を担うDOCK2という遺伝子領域の一塩基多型(SNP)が、65歳以下の非高齢者において約2倍の重症化リスクを有することを発見しました(図2)。さらに第4波・第5波で収集した約2,400名分のDNAでも、DOCK2のバリアントが重症化リスクとなることを確認しました。また、DOCK2(DOCK2という遺伝子から作られるたんぱく質)はリンパ球の遊走や抗ウイルス活性を有する1型インターフェロンの産生に重要な役割を担っていることが知られており、この点に注目し、さらに解析を進めました。
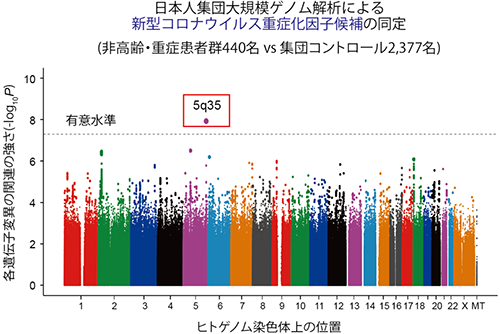
図2.日本人集団におけるCOVID-19重症化ゲノムワイド関連解析の成果
日本人COVID-19患者において、5番染色体上のDOCK2遺伝子近傍領域(5q35)の遺伝子多型が、65歳未満の非高齢者において約2倍の重症化リスクを有することを発見した。
DOCK2は重症COVID-19のバイオマーカーとなる
次に、実際のDOCK2発現量を調べるためにCOVID-19患者473人の血液を用いて、RNA-seq解析(細胞内の全転写産物・全RNAの定量を行う解析)を行いました。すると、COVID-19の重症化リスクとなる遺伝子のタイプをもつ患者さんではそれをもたない患者さんに比べ、また重症の患者さんでは非重症の患者さんと比べ、DOCK2の発現量が低下していました。
また、COVID-19患者さんの末梢血単核細胞を用いたsingle cell RNA-seq解析(一個の細胞に含まれる全転写産物の発現量を定量的に解析する手法)により、DOCK2は単球系という細胞集団で発現が高いことが確認されました。そして、重症COVID-19患者さんでは、健常者と比較して、この単球系の細胞集団でDOCK2の発現が特に低下していることが判明しました。
さらに、不幸にしてCOVID-19で亡くなられた方の肺を解析に用いさせていただき、DOCK2のたんぱく質レベルでの発現解析を行ったところ、COVID-19による肺炎では、一般的な細菌性肺炎に比べて、DOCK2の発現低下が確認されました。
以上のヒト検体を用いた検討から、DOCK2はCOVID-19の疾患感受性遺伝子であるだけでなく、重症化のバイオマーカーとなる可能性を見出しました。
SARS-CoV-2感染シリアンハムスターモデルはDOCK2の阻害により重症化
最後に、SARS-CoV-2感染動物モデルであるシリアンハムスターを用いてDOCK2の機能解析を行いました。DOCK2の阻害剤CPYPPをSARS-CoV-2感染シリアンハムスターモデルに投与すると、顕著な体重減少があり、重症肺炎が引き起こされることが分かりました。さらに、CPYPP投与群では、鼻腔・肺でウイルス量が増加しており、肺内のマクロファージが減少し、抗ウイルス活性に重要な役割を果たす1型インターフェロン応答は低下している一方、炎症性サイトカインは上昇していました。以上により、DOCK2は、SARS-CoV-2感染に対する免疫に重要な役割を果たしており、その機能を阻害するとSARS-CoV-2感染が重症化することが示されました。
今後の展開
本研究では、コロナ制圧タスクフォースが有するアジア最大のCOVID-19検体から、COVID-19の重症化遺伝子としてDOCK2を同定し、各種の機能解析によりDOCK2がCOVID-19の有望な治療標的となる可能性も明らかにしました。今後、DOCK2を活性化する薬剤が新たなCOVID-19の治療薬となることが期待されます。
コロナ制圧タスクフォースでは、同検体の遺伝子発現解析、たんぱく質発現解析、代謝産物の網羅的な解析、免疫応答の解析、ワクチンの開発などが進行中です。新型コロナウイルス感染症の克服に向け、新型コロナウイルス感染回復後の長期的な副作用の解析など、今後も引き続き、新型コロナウイルス感染症と闘う患者さんや、新型コロナウイルス感染症診療の最前線に立つ医療従事者とともに、新型コロナウイルス感染症の克服に向けて、最先端の解析技術を用いて、研究活動を続けていきます。また、新型コロナウイルス感染症制圧に向けた社会へのさらなる貢献を目指して、国の公共データベースを含めて、様々な機関と協力体制を広げていく予定です。
今回、コロナ制圧タスクフォースで得られた科学的知見もさることながら、COVID-19という未曽有のパンデミック下で、全国100以上の医療機関が集結して結成されたネットワークはコロナ制圧タスクフォースの唯一無二の財産となっています。今後、予想されるネクストパンデミックにおいて、社会に資する研究活動が展開できるように、よりレジリエントな研究体制の構築を模索していきます。
参考文献
The whole blood transcriptional regulation landscape in 465 COVID-19 infected samples from Japan COVID-19 Task Force.
Wang, Q.S. et al.
Nat Commun. 2022 Aug 22;13(1):4830. doi: 10.1038/s41467-022-32276-2.
DOCK2 is involved in the host genetics and biology of severe COVID-19.
Namkoong H, et al.
Nature. 2022 Sep;609(7928):754-760. doi: 10.1038/s41586-022-05163-5. Epub 2022 Aug 8.
最終更新日:2023年8月1日
記事作成日:2023年8月1日