脳脊髄を支える「ミエリン」
脳や脊髄はしばしば「神経細胞の塊」と誤解されていますが、ヒト脳の中で神経細胞が占める割合はたった1割に過ぎません。残る9割は神経細胞をサポートする様々な細胞(グリア細胞)によって占められています。このうちオリゴデンドロサイトと呼ばれる細胞は、神経細胞の突起(軸索)に「ミエリン」と呼ばれる膜を巻きつける役割を担っています(図1)。
ミエリン(別名、髄鞘)はオリゴデンドロサイトの細胞膜が延長しバウムクーヘンのように巻き付いた構造物です。このミエリンによって、軸索を流れる信号の速度が約100倍加速されることが知られています。さらにミエリンは軸索を通じて神経細胞に栄養も供給しています。ヒト脳のミエリンの大半は出生後に構築されますが、例えばピアノの練習をすると、その分だけミエリンも増えることが知られています。我々が学習し成長できるのもミエリンのお陰といっても過言ではありません。
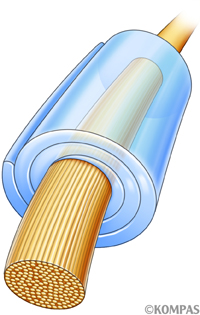
図1.神経軸索を包むミエリン
ミエリンが剥がれる「脱髄疾患」
ヒト脳では50歳前後までミエリンは増え続け、日々の成長を支えていることが知られています。このミエリンが何らかの理由で壊れてしまう疾患を脱髄疾患といい、特に代表的な脱髄疾患としては多発性硬化症が挙げられます。多発性硬化症は主に20歳から30歳の女性を侵す原因不明の難病で、脳や脊髄のミエリンが壊れることで、麻痺や感覚障害、場合によっては失明や認知機能の低下なども引き起こします(図2)。多発性硬化症を治療せずに放置すると多くの患者さんは徐々に進行し車椅子や寝たきりになってしまいます。幸いにして多発性硬化症では脱髄を食い止める様々な治療薬が開発されてきており、早期に診断し早期に治療を開始することで、障害の進行を食い止めることができるようになってきています。さらにはミエリンを再生させる治療薬の開発も世界中で進められており、近い将来には壊れたミエリンを再生させ、症状を改善させることができるようになると期待されています。
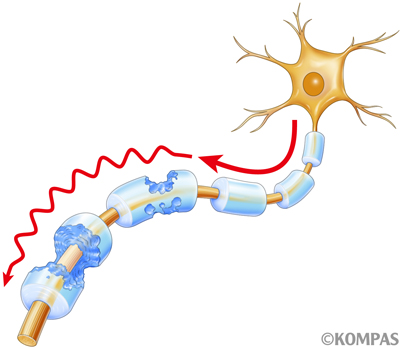
図2.脳や脊髄のミエリンが破壊された状態
既存のMRIではミエリンが見えない
脳や脊髄は直接検査をすることが難しい臓器で、よほどの事情がなければ生検などは行いません。従って、各種診断のためにはMRIを用いて検査することが一般的になっています。MRIは簡単には水分の分布を見る方法に過ぎず、ミエリン自体を見ることはできません。例えば、MRIで「水っぽくなっている場所」が多発している際には多発性硬化症を診断しているのが実情ですが、本当にミエリンが壊れているかどうかは現在のMRI技術では確認できていません。あるいは治療によってミエリンが再生したとしても、これまでのMRIではそれを見ることはできませんでした。これはミエリンを再生させる治療薬の開発において大きな課題となっていました。
MRIを駆使してミエリンを可視化する「ミエリンマップ法」
MRIは患者さんの負担が少なく、とても安全な検査方法です。そこで我々はなんとかMRIを応用してミエリンを可視化することができないかと考えました。放射線科、生理学教室、整形外科、神経内科のそれぞれ専門家が合同チームを組み、試行錯誤を経て、ついにミエリンを可視化するMRIの新しい撮像法として「ミエリンマップ法」を開発することに成功しました。ミエリンマップ法は当院で日常的に使用しているMRI装置(3テスラ装置)を用いてわずか10分弱で撮影可能であります(図3)。
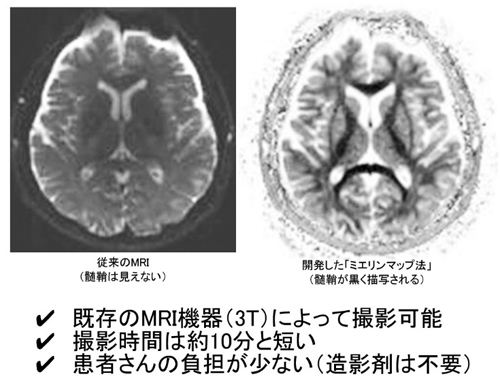
図3.MRI(3テスラ装置)によりミエリン可視化に成功
今後の展開
脳や脊髄のミエリンが容易に可視化できるようになったことで、多発性硬化症などの脱髄疾患をより早期に診断し、治療の適正化を判断できるようになる可能性があります。また昨今ミエリンの異常が指摘されてしている、アルツハイマー病、筋萎縮性側索硬化症などの神経変性疾患や、統合失調症や躁うつ病などの精神疾患などの研究に役立つ可能性があります。さらには慶應義塾大学医学部が推進している神経領域における再生医療の実現化において、それら治療の効果判定に有用である可能性があります。これらを実現化する第一歩として、すでに慶應義塾大学病院に通院されている多発性硬化症患者さんを対象とした臨床研究が始まっています。
参考文献
Application of q-Space Diffusion MRI for the Visualization of White Matter.
Fujiyoshi K, Hikishima K, Nakahara J, Tsuji O, Hata J, Konomi T, Nagai T, Shibata S, Kaneko S, Iwanami A, Momoshima S, Takahashi S, Jinzaki M, Suzuki N, Toyama Y, Nakamura M, Okano H.
J Neurosci. 2016 Mar 2;36(9):2796-808.
http://www.jneurosci.org/content/36/9.toc

左:筆者 |
|
中央(左から): |
藤吉兼浩(国立病院機構村山医療センター) |
右:疋島啓吾(沖縄科学技術大学院大学、生理学教室訪問研究員) |
|
最終更新日:2016年8月1日
記事作成日:2016年8月1日