急性腎障害とは
急性腎障害は、重症の感染症や心臓・血管の手術後などで頻繁に生じる合併症です。その発症率を調査した研究では、病院の集中治療室に入院する患者さんの10%以上に急性腎障害が認められ、その生存率はほぼ50%と報告されています。急性腎障害の発症・進展には、腎臓に存在する多くの種類の細胞が関わっていることが判明しており、血管の内皮細胞や尿の濃縮・希釈に働く尿細管細胞、さらには血液中を循環して炎症に関与する好中球やリンパ球、マクロファージなどが研究されていますが、現在のところ、有効な治療薬は確立していません。
血管内皮細胞に発現するKLF4のはたらき
細胞の分化や増殖にかかわる遺伝子の発現量を調節する転写因子であるKrüppel-like factor 4 (KLF4) は、皮膚や胃・腸の細胞分化を調節したり、がん細胞の増殖に関与することが分かっています。また、京都大学の山中教授らが開発した人工多能性幹細胞 (iPS細胞) の作製に必要な4因子のうちの1つとしても、近年大きな注目を集めています。KLF4は血管では内皮細胞に発現しています。血管が傷害を受けた場合、血管は肥厚・増殖しはじめますが、KLF4が欠損していると血管の肥厚・増殖が過剰になることを、我々は報告しました(文献1)。その後の研究では、血管内皮細胞で選択的にKLF4を欠損させても、血管傷害に対して同様の肥厚・増殖がみられることを示しました(文献2)。さらに分子メカニズムとして、血管内皮細胞のKLF4が、炎症を引き起こす細胞接着因子の量を調節し、血液中を流れる炎症細胞が傷害部位に集積することを制御していること、さらにKLF4の欠損した状態ではその制御が効かないために炎症が過剰になってしまうという機序を解明しました。
スタチンはKLF4を介して急性腎障害を軽減させる
先に述べたように、急性腎障害の発症過程においても血管内皮細胞や血液中の炎症細胞は重要な役割を果たしています。そこで我々は、急性腎障害に対しても血管内皮細胞のKLF4が障害を抑制する方向に働くのではないかとの仮説を立てて、研究を行いました。また、コレステロールが高くなる脂質異常症の治療薬として用いられているスタチンには、多面的な作用があり心血管病の発症を抑える作用がありますが、その効果はKLF4の作用と似ています。そこで、スタチンの急性腎障害への関与についても検討しました(文献3)。
マウスの腎臓の血流を少なくした後に血流を戻すという操作をすると、虚血再灌流障害という急性腎障害が生じます。具体的には、麻酔の下で開腹し、腎臓に酸素と栄養成分を運ぶ動脈を約30分間、一時的にクリップで閉じる処置をします。クリップを外すと腎臓への血流が再開しますが、この処置を受けたマウスでは、腎臓の障害がおき始め、障害を表す血液マーカーの値が上昇したり、腎臓においては一部の尿細管細胞が死んでしまったり、炎症細胞が集まったりすることがみられます。今回、血管内皮細胞のKLF4を欠損したマウスと、KLF4を欠損していないマウスの腎臓に、虚血再灌流の操作を行い障害の程度を比較したところ、KLF4欠損マウスで、障害がより強く観察されることを発見しました。さらに、スタチンを3日間投薬した後に腎臓の虚血再灌流障害を引き起こしてみたところ、通常のマウスではスタチンを投与しておくことによって急性腎障害が軽減しましたが、KLF4欠損マウスではスタチンによる軽減効果を認めませんでした。
培養した血管内皮細胞を用いてそのメカニズムを検討してみると、スタチンはKLF4が現われる量を増加させることで、好中球などの炎症細胞を引き寄せるのに必要な細胞接着因子の発現を抑制することが明らかとなりました。
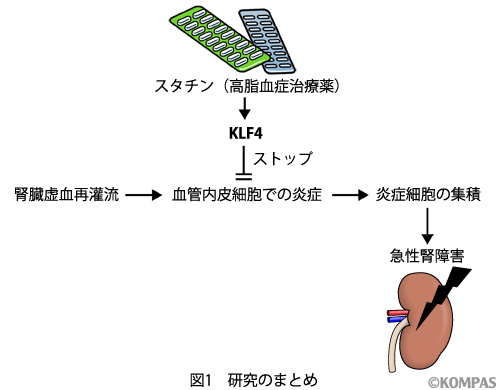
これらの実験結果は、虚血再灌流に対してスタチンを投与しておくと、KLF4を介した働きによって細胞接着因子の発現が抑えられることから腎臓の炎症が軽減されますが、KLF4が欠損している状況ではスタチン薬を前投与しても、虚血再灌流に伴った細胞接着因子の発現が過剰となり、その結果、炎症細胞が集積し、それによる腎障害が現れることを示しています(図1)。
今後の展開
今後、ヒトにおいても急性腎障害に対するスタチンの有効性を検証していくことが期待されます。また、KLF4が腎障害を抑制することが明らかになったことにより、KLF4を標的とした新たな治療薬が開発され、急性腎障害の発生が軽減・予防されることが期待されます。
参考文献
- Conditional deletion of Krüppel-like factor 4 delays downregulation of smooth muscle cell differentiation markers but accelerates neointimal formation following vascular injury.
Yoshida T, Kaestner KH, Owens GK.
Circ Res. 2008 Jun 20;102(12):1548-57. doi:10.1161/CIRCRESAHA.108.176974. Epub 2008 May 15.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2633447/
- Deletion of Krüppel-like factor 4 in endothelial and hematopoietic cells enhances neointimal formation following vascular injury.
Yoshida T, Yamashita M, Horimai C, Hayashi M.
J Am Heart Assoc. 2014 Jan 27;3(1):e000622.
doi: 10.1161/JAHA.113.000622.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3959705/
- Endothelial Krüppel-Like Factor 4 Mediates the Protective Effect of Statins against Ischemic AKI.
Yoshida T, Yamashita M, Iwai M, Hayashi M.
J Am Soc Nephrol. 2015 Oct 15. pii: ASN.2015040460. [Epub ahead of print] doi:10.1681/ASN.2015040460
http://jasn.asnjournals.org/content/early/2015/10/14/ASN.2015040460.abstract?sid=5b69c19f-af57-4d57-af02-0e4cb95e33eb

左:筆者、右:山下真帆(研究員:文献2,3の共著者)
最終更新日:2015年12月21日
記事作成日:2015年12月21日