がんに深く関わる「腫瘍微小環境」
がん組織は、がん細胞とそれを支える間質と呼ばれる成分から構成されています。間質は、線維芽細胞と呼ばれる細胞、血管やリンパ管を形成する細胞、炎症をつかさどる細胞などの多種類の細胞、さらにこれらの細胞間に存在するコラーゲン(膠原線維)などの細胞外マトリックスおよびそれに結合する生理活性物質(増殖因子、サイトカイン、ケモカインなど)などからなります。これらの間質は腫瘍微小環境(tumor microenvironment)と呼ばれ、がん細胞が住みやすい環境を形成しています。これまでのがん研究の多くはがん細胞のみを対象とし、間質成分は軽視される傾向にありましたが、最近この腫瘍微小環境ががん細胞の生存や増殖に深く関わっていることが明らかになり、新しいがん診断や治療標的として注目されつつあります。
がん関連線維芽細胞(CAF)の出現
がん間質を構成する重要なものに線維芽細胞があります。一般的に、線維芽細胞は体のいろいろな場所に存在していて、コラーゲンなどの線維をつくり出すことによって組織を構築するほか、けがをした際には傷口を修復する役割をもつ細胞として知られています。ところが、線維芽細胞に異常な活性化がおこると、細胞外マトリックスが過剰に産生され、正常な構造を破壊されるなど、さまざまな病態の悪化がおこります。
がんにおいても、特に悪性度が高いがんでは、異常に活性化した特殊な線維芽細胞が多く出現することが報告され、「がん関連線維芽細胞(cancer-associated fibroblast:CAF)」と呼ばれています。これらのCAFは血管新生やがん細胞の増殖・浸潤などを促進することがわかってきました(文献1)(図1)。さらに、最近の研究からCAFががん細胞の化学療法や放射線治療に対する抵抗性を強めることも明らかとなってきており、CAFをはじめとする間質を制御することはがんを治療するうえでとても重要と考えられます。しかしながら、CAFの発生機序やがん細胞との相互作用のメカニズムについてはわかっていない部分が多く、がん間質に対する分子生物学的な治療法については未だに確立されていないのが現状です。
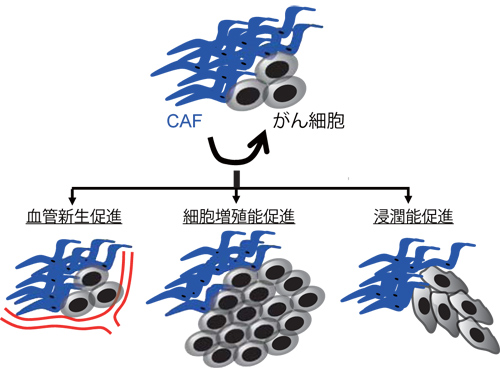
図1:がん関連線維芽細胞(cancer-associated fibroblast: CAF)は血管新生やがん細胞の増殖・浸潤などを促進します。(文献1の図より著者改変)
CAFを制御するTIMP分子
我々は近年TIMP (tissue inhibitor of metalloproteinases)という分子が、がん間質の主要な構成成分であるCAFの機能を抑制していることを明らかにしました。TIMPはメタロプロテアーゼと呼ばれる酵素を阻害する分子です。がんなどの病的組織においては、細胞外マトリックスを分解するメタロプロテアーゼとその阻害因子であるTIMPのバランスが崩れることにより組織内微小環境が大きく変化することが知られています。
この研究では、Timp欠損マウスの解析を行うことにより、Timp欠損線維芽細胞がメタロプロテアーゼ活性依存性にCAFに類似した活性化した線維芽細胞様形質を示すことを見出しました。さらに、Timp欠損線維芽細胞を種々のがん細胞と混合してマウスに移植した群では、がん細胞のみ移植の群あるいはがん細胞と正常線維芽細胞を混合した群と比べて、腫瘍が有意に増大するとともに肺への転移も多く認められました。このことより、生物学的にもTimp欠損線維芽細胞がCAFと同様の作用を示すことがわかりました。
これまでに、CAFががん細胞に作用する際の細胞間コミュニケーション媒体として主にサイトカインなどの分泌タンパク質が報告されていましたが、今回我々は線維芽細胞が産生するエクソソーム(exosome)と呼ばれる顆粒の中にがんを活性化するさまざまなタンパクが含まれていることを見出し、線維芽細胞由来エクソソームががん細胞の運動性を亢進させたり、がん幹細胞と呼ばれるより悪性度の高いがん細胞の維持に関与していることを明らかにしました(文献2)(図2)。エクソソームはタンパク質、mRNA、miRNA(マイクロRNA)といったさまざまな物質が含有することから、新たな細胞間のコミュニケーション媒体として最近注目されています(文献3)。がん細胞と間質細胞の相互作用においてもエクソソームが重要な因子になりうると推測されます。
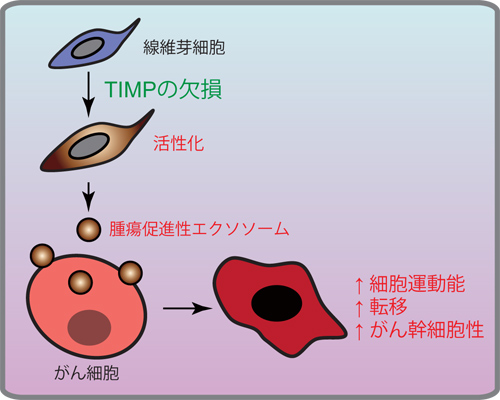
図2:Timp欠損線維芽細胞は活性化した線維芽細胞様形質を示すとともに、腫瘍促進性エクソソーム産生を介してがん細胞の運動能や転移を促進、さらにはがん幹細胞維持にも関わります。(文献2の図より著者改変)
がん間質を標的とした治療戦略
近年、顕微鏡下にレザー光で特定の細胞集団をとりだし研究するマイクロダイセクション法を用いた検討から、乳がん間質における遺伝子発現パターンが独立した予後予測因子となりうることが報告されてきました。そして、がん間質からのシグナルが直接的あるいは間接的にがん細胞に影響を及ぼし、腫瘍の増殖・進展に積極的に関与していることが推測されています。従来のがん治療の多くは増殖能の高いがん細胞を標的とした治療法が主体でしたが、遺伝的異常の頻度が高く、薬剤耐性を獲得しやすいがん細胞に比較して、間質を標的とした治療は治療抵抗性を生じにくいとも考えられます。がん間質の基礎的な研究がさらに発展することで、今後はこれらを標的とした新たな治療戦略が確立されることが期待されます。
参考文献
- Carcinoma-associated fibroblasts are a rate-limiting determinant for tumour progression.
Shimoda M, Mellody KT, Orimo A.
Semin Cell Dev Biol. 2010 Feb;21(1):19-25. doi: 10.1016/j.semcdb.2009.10.002. Epub 2009 Oct 24.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2828545/
- Loss of the Timp gene family is sufficient for the acquisition of the CAF-like cell state.
Shimoda M, Principe S, Jackson HW, Luga V, Fang H, Molyneux SD, Shao YW, Aiken A, Waterhouse PD, Karamboulas C, Hess FM, Ohtsuka T, Okada Y, Ailles L, Ludwig A, Wrana JL, Kislinger T, Khokha R.
Nat Cell Biol. 2014 Sep;16(9):889-901. doi: 10.1038/ncb3021. Epub 2014 Aug 24.
http://www.nature.com/ncb/journal/v16/n9/abs/ncb3021.html
- Proteolytic factors in exosomes.
Shimoda M, Khokha R.
Proteomics. 2013 May;13(10-11):1624-36. doi: 10.1002/pmic.201200458.
http://onlinelibrary.wiley.com/doi/10.1002/pmic.201200458/abstract

左から、岡田保典(病理学教室教授)、下田将之(病理学教室講師)、大塚崇(外科学教室講師)
最終更新日:2014年12月5日
記事作成日:2014年12月5日