はじめに
炎症性腸疾患とは、潰瘍性大腸炎、クローン病に代表される消化管に慢性的に炎症が起こる原因不明の疾患群で、今なお、病気を根本的に治すいわゆる「根治療法」が存在せず、厚生労働省により難病に指定されています。しかし、近年のめざましい検査・治療法の進歩に伴い、寛解状態(病気の活動性が落ち着いている良好な状態)を長期にわたって維持することで、大きな制限を受けることなく、通常の生活を送ることが可能になってきています。ここでは、慶應義塾大学病院における炎症性腸疾患の診療の試みをご紹介します。
当院における炎症性腸疾患の診療の実際
当院では、炎症性腸疾患を専門とする医師が多数在籍し、幅広い患者さんに対応できるよう、月曜日から土曜日(第1・第3土曜は休診日)まで毎日、専門外来および専門医師による大腸内視鏡検査を実施しています。また、内視鏡センター、放射線診断科と協力し、血液検査、便検査、大腸内視鏡検査・バルーン小腸内視鏡、小腸造影検査、カプセル内視鏡、MRエンテログラフィーなどの中から適切な検査方法を選択し、病状を適切に評価して治療を行っています。
病状評価の中心は、内視鏡所見で粘膜(腸管の表面)の炎症が改善していることですが、内視鏡検査は頻繁に行うことは困難ですので、それを補うために、外来にて血液検査(CRPやLRG(ロイシンリッチα2グリコプロテイン)など)、便の検査(便中カルプロテクチンなど)を組み合わせて負担の少ない検査を行っています。
現在、炎症性腸疾患では、基本薬である5-アミノサリチル酸(5-ASA)製剤をはじめ、副腎皮質ステロイド、チオプリン製剤(免疫調節薬)、栄養療法(クローン病のみ)が治療に用いられています。これらの治療で十分に寛解が得られない患者さんには、生物学的製剤(クローン病 4種類、潰瘍性大腸炎 5種類)、経口ヤヌスキナーゼ(JAK)阻害薬(潰瘍性大腸炎 2種類)、経口インテグリン阻害薬(潰瘍性大腸炎 1種類)が使用されることがあります。近年、炎症性腸疾患の治療薬の開発はめざましく、過去3年間(2022年5月現在)で潰瘍性大腸炎では3種類 (抗インターロイキン12/23 p40抗体製剤、JAK-1阻害薬、経口インテグリンα4阻害薬)、クローン病では1種類 (抗インテグリンα4β7抗体製剤) が新たな治療選択肢として加わりました。
当科では、多くの患者さんが必要な治療をスムーズに受けられるよう、免疫統括医療センターと連携を行っています。同センター内に併設されている治療室において、生物学的製剤を中心とした専門性の高い治療を患者さんに提供しています。さらに、病状の変化が生じた場合など、必要に応じて当日に別の治療に変更するといった迅速な対応も、可能な限り臨機応変に行っています*。
*病状や状況などによって可能な場合に限ります。
内科的治療(薬物による治療)で十分に効果が得られず、腸管の狭窄が起こった際には、狭窄の形状によっては内視鏡的バルーン拡張術により、内視鏡で狭窄を広げることで手術を回避するという選択肢もあります。外科的治療が必要な場合も、手術中に内視鏡で小腸を観察するなど精査してなるべく腸の切除範囲を狭められるよう、外科の医師とも緊密に連携して診療を行っています。
近年注目されているTreat to Target という考え方
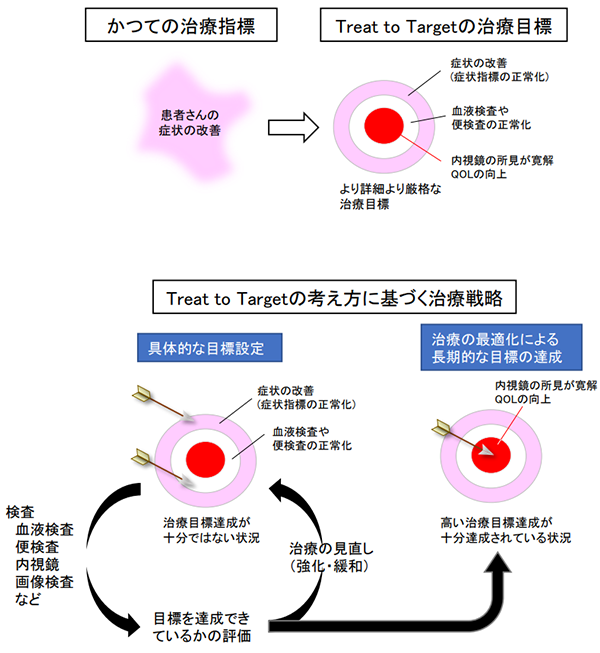
炎症性腸疾患領域では、近年Treat to Target(T2T:目標達成に向けた治療)という概念が提唱されています。かつては、患者さんの症状や血液検査の結果などをもとに、「患者さんが困っていない」「医師が問題ない」と判断されれば治療は「問題ない」とされていました。しかし、この「問題ない」という判断が医師によって異なる可能性や、自覚症状や血液検査の結果に異常がないだけで本当に十分なのか、といったことに関心が集まるようになりました。
こうした問題に対して、具体的な治療目標を設定し、治療によってそれを達成できているのかどうかの評価を行い、達成できていなければ治療の見直しを行って再び評価を行う、という治療戦略が世界的に掲げられるようになりました。これがTreat to Target という考え方です。
2021年に、米国消化器病学会が刊行する学術論文雑誌であるGastroenterology誌にこのTreat to Targetに関するステートメントの改訂(STRIDE-II)が発表されました(文献1)。この中では、患者さんの自覚症状や状態を客観的な指標(Patient-reported outcome-2 (PRO-2)スコアやpartial Mayo スコア、Crohn’s disease activity index (CDAI)スコアなどの指標が確立されています)を用いて評価し、短期的な目標としてこれらの指標の改善を目指し、中期的な目標として自覚症状よりも病気の状態をより反映すると考えられている便中カルプロテクチン検査の正常化や、小児の患者さんにおいては正常な成長が得られることを目指します。そして長期的な目標として内視鏡的な寛解と生活の質(Quality of Life:QOL)の向上を目指します。
炎症性腸疾患では自覚症状や血液検査に異常がなくても、腸の中に炎症が残っているということがしばしばあります。このような状態が長く続くと、腸に狭い箇所(狭窄)ができたり、炎症部分からがんが発生したりする恐れがあります。こうした問題を防ぐためには、実際に内視鏡検査で炎症がない状態(寛解状態)を達成する必要があることから、長期的な目標として内視鏡的な寛解を目指します。そして、治療を受ける患者さんのQOLを高めることもまた、治療のゴールとして重要であると考えています。
当院の炎症性腸疾患専門外来では、こうしたTreat to Targetの考え方をはじめとした最新の知見(エビデンス)に基づいた診療を実践しています。
最新の取り組み
潰瘍性大腸炎関連発がんのサーベイランス(経過観察)
潰瘍性大腸炎患者さんの大腸がんの発がんリスクは、その他の方よりも高いことが疫学調査により明らかになっています。内視鏡の機械が進歩した現在でも早期に発見することが極めて困難な中で、我々は世界に先駆けて潰瘍性大腸炎患者さんに発症する大腸がんの分子病理学的な特徴に着目し(文献2,3)、リスク患者を選別しながら注意深いサーベイランスを行っています。大腸がんが発見された場合にも、内視鏡センター、腫瘍センター低侵襲治療部門、一般・消化器外科、放射線診断科、病理診断科などとも連携して、他分野の医師と協議した上で治療の選択肢をご提案します。
難治性潰瘍性大腸炎に対する青黛の有用性と安全性の検討
青黛は、植物から抽出したインジゴを含有する生薬で、主に藍染の染料として用いられてきました。中国では、古くから潰瘍性大腸炎に対して青黛を含む漢方薬が用いられていましたが、十分な科学的検証がなされていませんでした。
当院では、世界で初めて潰瘍性大腸炎の患者さんに対する青黛の有効性と安全性を検証するために前向き臨床試験を行い、投与後8週間に従来の治療薬に反応しなかった難治例を含めて約7割の患者さんに有効であることを報告しました(文献4)。また、その薬効についての検討を行い、青黛が腸管の免疫を抑える細胞を増やすことを明らかにする(文献5)など、科学的な検証を進めています。
一方で、青黛および青黛含有漢方薬を使用した患者の全国調査により、特に長期投与されていた患者さんで原発性肺高血圧症という心臓から肺に血液を送る肺動脈の血圧が高くなり、心臓に負担がかかる難知性の病気が発生するなど副作用の存在が明らかになっています(文献6)。そのことを十分に認知せずに青黛を含む漢方薬を自己判断や自由診療で内服、処方している患者さんや医師がいるという社会的な問題点も指摘されていました。
当院で行った青黛を8週間投与した臨床試験では、原発性肺高血圧症は認められませんでした。青黛は、その用法用量・使用期間や適応などについて十分な医学的知識に基づいて使用をすることで、寛解導入療法としての新たな選択肢となる可能性があります。
現在消化器内科では、青黛の安全な治療薬としての実用化を目指して、「実臨床における難治性潰瘍性大腸炎に対する青黛の有用性と安全性の検討(青黛実用化試験)![]() 」を実施しています。当院に通院されていない患者さんでも、かかりつけの先生に診療していただきながら、治験の期間だけ当院に通院いただくことも可能です。これらの取り組みにご興味をお持ちの患者さんは、主治医と必ずご相談の上、受診をご検討ください。
」を実施しています。当院に通院されていない患者さんでも、かかりつけの先生に診療していただきながら、治験の期間だけ当院に通院いただくことも可能です。これらの取り組みにご興味をお持ちの患者さんは、主治医と必ずご相談の上、受診をご検討ください。
最後に
炎症性腸疾患の検査・治療法が多様化する中で、慶應義塾大学病院消化器内科では、炎症性腸疾患を専門とする医師が多く所属し、炎症性腸疾患の患者さんの診療にあたっています。月曜から土曜日まで炎症性腸疾患を専門とする医師が外来、内視鏡検査を担当しており、症状が悪化(再燃)する患者さんをいつでも診療できる体制を整えています。内視鏡センター、一般・消化器外科、放射線診断科、腫瘍センターなどの関連部門とも協力して患者さんに最適な治療を提供いたします。
参考文献
-
STRIDE-II: An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organization for the Study of IBD (IOIBD): Determining Therapeutic Goals for Treat-to-Target strategies in IBD.
Turner D, Ricciuto A, Lewis A, et al.
Gastroenterology. 2021 Apr;160(5):1570-1583. doi: 10.1053/j.gastro.2020.12.031. -
Epithelium Replacement Contributes to Field Expansion of Squamous Epithelium and Ulcerative Colitis-Associated Neoplasia.
Sugimoto S, Iwao Y, Shimoda M, Takabayashi K, Sato T, Kanai T; Keio IBD Collaborators.
Gastroenterology. 2022 Jan;162(1):334-337.e5. doi: 10.1053/j.gastro.2021.09.051.
-
Somatic inflammatory gene mutations in human ulcerative colitis epithelium.
Nanki K, Fujii M, Shimokawa M, Matano M, et al.
Nature. 2020 Dec;577(7789):254-259. doi: 10.1038/s41586-019-1844-5. - Efficacy of Indigo Naturalis in a Multicenter Randomized Controlled Trial of Patients With Ulcerative Colitis.
Naganuma M, Sugimoto S, Mitsuyama K, et al.
Gastroenterology. 2018 Mar;154(4):935-947. doi: 10.1053/j.gastro.2017.11.024. -
Aryl hydrocarbon receptor signals in epithelial cells govern the recruitment and location of Helios+ Tregs in the gut.
Yoshimatsu Y, Sujino T, Miyamoto K, et al.
Cell Rep. 2022 May 10;39(6):110773. Doi: 10.1016/j.celrep.2022.110773. -
The use of traditional and newer calcineurin inhibitors in inflammatory bowel disease.
Naganuma M, Fujii T, Watanabe M.
J Gastroenterol. 2011 Feb;46(2):129-37. doi: 10.1007/s00535-010-0352-z.
関連リンク
文責:消化器内科![]()
執筆:三上洋平、清原裕貴
最終更新日:2022年7月29日
記事作成日:2022年7月29日