概要
日本人のがんによる死亡者数の中で、肺がんはがん死因の第1位です。肺がんと新たに診断される人数は、1年間に10万人あたり88.7人であり、毎年7万人以上が肺がんで亡くなっています。男女別の罹患率でみると、男性は女性2倍以上になっています。肺がんは喫煙との関連が、非常に大きいがんであり、たばこを吸わない人に比べて、吸う人が肺がんになるリスクは男性で4.4倍、女性で2.8倍です。また、たばこを吸わない人でも、周囲に流れるたばこの煙を吸うこと(受動喫煙)により肺がんになる危険性が高まることも報告されています。禁煙は肺がんの最も有効な予防法です。喫煙以外では大気汚染やアスベストなどへの暴露も重要な要因と考えられています。また、もともと間質性肺炎、慢性閉塞性肺疾患(COPD)などを持っている方は、肺がんを発症しやすいことが知られています。
症状
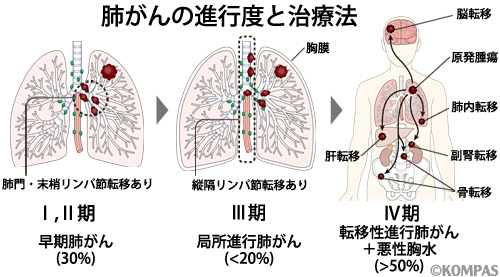
肺がんはほかのがんに比べて、比較的進行しやすく、ほかの臓器に転移しやすいという特徴があります。症状としては大きく分けて、肺がんが周りに拡がっていくことで出てくる肺・気管支の症状と、転移により侵された臓器(多くは脳、骨、肝臓、副腎など)の障害による症状とに分けられます。前者としては、咳や血の混じった痰、胸の痛み、息苦しさ、発熱などが代表的な症状ですが、がんの生じる場所によっては、しゃがれ声、しゃっくり、顔のむくみや動悸などを認めることもあります。後者としては骨への転移による痛みや、脳への転移による頭痛、吐き気、麻痺、けいれんや意識障害などがあります。ただし、症状は肺がんが比較的進行している患者さんに見られることが多く、初期は全く無症状で、検診や他の病気で受診した際に、胸部レントゲン写真などにより偶然に発見されることも少なくありません。
診断
肺がんの診断では、各種画像検査と組織(病理)診断を得るための検査を組み合わせて、最終的な組織型と病気の進行具合(病期)を決定し、それにしたがって治療方針を決定します。肺がんの組織型としては、腺がん、扁平上皮がん、大細胞がん、小細胞がんの4つが主ですが、小細胞肺がんは進展速度が速く、初期から他臓器へ転移しやすいなどの特徴があり、治療法も異なるため、それ以外のがんをひっくるめて非小細胞肺がんとして区別します。補助的な診断として、CEA、CYFRA(シフラ)、ProGRP、NSEなどの腫瘍マーカーがあり、治療効果の判定、再発の予知に有効なことがあります。しかし、腫瘍マーカーは早期がんでは異常を示さないことが多く、早期発見には不向きです。
- 画像検査(病期診断):画像検査により肺がんの部位、大きさ、拡がり(周囲への進展具合や他臓器への転移)およびリンパ節転移の有無を調べ、病期分類(表1)を行います。
- 胸部X線:最も基本的な「胸のレントゲン写真」検査です。
- 胸部CT:コンピュータ断層撮影です。X線では分からないがんの正確な部位、大きさ、周囲臓器への拡がりやリンパ節への転移の有無などを調べます。
- 腹部CT:肝臓や副腎など腹部の臓器への転移の有無を調べます。
- 頭部MRI・CT:脳への転移の有無を調べます。
- 骨シンチグラフィー:骨への転移の有無を調べます。
- PET-CT:血管内に注射した放射性薬剤(18F-FDG)の分布と、CTを組み合わせて病変を診断します。縦隔リンパ節や他の臓器への転移の有無を調べます。
- 胸部X線:最も基本的な「胸のレントゲン写真」検査です。
- 組織診断:がんそのものから組織を採取して組織型を調べますが、その主な検査方法には次のものがあります。
- 気管支鏡:肺がんの診断に多く用いられる検査で、直径4〜6mm程度の円筒状の柔らかいファイバーをのどに麻酔をした後、口または鼻から挿入し、気管から気管支へと進め、生検鉗子等を用いて目的の場所から組織を採取します。従来の方法では、がんのある場所に生検器具等を正確に到達させることが困難な場合がありました。当院では、超音波内視鏡、バーチャル気管支鏡、自家蛍光電子内視鏡など、最新のツールを用いて診断向上に努めています。
- 経皮的肺生検(CTあるいはエコーガイド下):気管支鏡での組織採取が困難な場合は、CTあるいはエコーを用いてリアルタイムで病変の影を見ながら、生検用の針を体の外から刺して組織を採取することもあります。
- 開胸生検:気管支鏡やCTガイド下生検でも確定診断が得られない場合は、診断と治療を兼ねて全身麻酔をして病巣部を触診し、針生検や肺部分切除を行い、確定診断をつけることがあります。肺がんの診断が得られた場合は、そのまま肺がん根治術を追加することもあります。
- バイオマーカーの検索:最近では、抗がん剤による治療を行う前に、がん細胞の遺伝子検査と組織型の診断をきちんと行い、より良い治療法を選ぶことが重要となっています。分子標的治療薬や一部の抗がん剤では、上皮増殖因子受容体(EGFR)などの遺伝子変異(異常)の有無や組織型により、その効果と副作用に差があることが分かっています。また、免疫チェックポイント阻害薬を投与する前には、がん組織におけるPD-L1というたんぱく質を確認する必要があります。
表1. 肺がんの臨床病期分類(UICC第8版, 2017年)
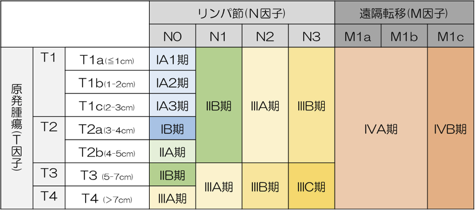
T因子-原発腫瘍
- T1:腫瘍の充実成分径≦3cm、肺または臓側胸膜に覆われている、葉気管支より中枢への浸潤が気管支鏡上認められない(すなわち主気管支に及んでいない)
- T1mi:微小浸潤性腺がん:部分充実型を示し、充実成分径≦0.5cmかつ病変全体径≦3cm
- T1a:充実成分径≦1cmでかつTis・T1miには相当しない
- T1b:充実成分径>1cmでかつ≦2cm
- T1c:充実成分径>2cmでかつ≦3cm
- T2:充実成分径>3cmでかつ≦5cm、または充実成分径≦3cmでも以下のいずれかであるもの
- 主気管支に及ぶが気管分岐部には及ばない
- 臓側胸膜に浸潤
- 肺門まで連続する部分的または一側全体の無気肺か閉塞性肺炎がある
- T2a:充実成分径>3cmでかつ≦4cm
- T2b:充実成分径>4cmでかつ≦5cm
- T3:充実成分径>5cmでかつ≦7cm、または充実成分径≦5cmでも以下のいずれかであるもの
- 臓側胸膜、胸壁(superior sulcus tumorを含む)、横隔神経、心膜のいずれかに直接浸潤
- 同一葉内の不連続な副腫瘍結節
- T4:充実成分径>7cm、または大きさを問わず横隔膜、縦隔、心臓、大血管、気管、反回神経、食道、椎体、気管分岐部への浸潤、あるいは同側の異なった肺葉内の副腫瘍結節
N因子-所属リンパ節
- NX:所属リンパ節評価不能
- N0:所属リンパ節転移なし
- N1:同側の気管支周囲かつ/または同側肺門、肺内リンパ節への転移で原発腫瘍の直接浸潤を含める
- N2:同側縦隔かつ/または気管分岐下リンパ節への転移
- N3:対側縦隔、対側肺門、同側あるいは対側の前斜角筋、鎖骨上窩リンパ節への転移
M因子-遠隔転移
- M0:遠隔転移なし
- M1:遠隔転移がある
- M1a:対側肺内の副腫瘍結節、胸膜または心膜の結節、悪性胸水(同側・対側)、悪性心嚢水
- M1b:肺以外の一臓器への単発遠隔転移がある
- M1c:肺以外の一臓器または多臓器への多発遠隔転移がある
治療
肺がんの治療には、大きく分けて手術療法、放射線療法、薬物療法の3つの選択肢があります。実際には組織型と病期をもとに、これらを単独で、あるいは組み合わせて治療を行います。
- 手術療法
早期の非小細胞肺がんに対する治療の中心は手術であり、現時点においては治癒をもたらす可能性が最も高い治療法です。
- 適応:手術が行われるためには「がんが手術で取りきることが可能な病期(表1の主にI~Ⅱ期)」であることと、「手術に耐えられ、かつ術後の生活の質が保たれると予想される全身状態」であることが必要です。これら2つの条件が満たされれば、高齢であっても手術を受ける患者さんはいます。
- 術式(手術方法):標準的な方法は病巣を含む肺葉の切除と周囲の領域リンパ節(肺門及び縦隔リンパ節)の郭清(切除)です。
- 成績:非小細胞肺がんに対して手術を受けた患者さんの5年生存率は手術後の病期分類(病理病期)がIA期では80%以上ですが、II期やIII期では未だによくありません。術後の予防的な化学療法(補助化学療法)が生存率をわずかながら(5〜10%程度)改善することが過去の研究から報告されており、病理病期IB、II、III期の患者さんでは術後に化学療法を追加する場合があります。
- 放射線療法
- 通常の放射線治療
直線加速器(リニアック)と呼ばれる大型の機械で、体の外から体内の病巣部に放射線を当てます。通常は、1日1回、土日と祝日を除いた毎日(週5回)の治療を約6週間かけて行います。治療が必要な範囲の形に合わせた照射範囲に対して正確に放射線をあてるために、専用のコンピュータを用いて、最適な計画を選択します。化学療法と組み合わせることもあります。 - 定位的放射線治療
患者さんの体を専用の枠でしっかりと固定して位置のずれがないようにして、病巣に対し多方向から放射線をピンポイントに集中させる方法です(図1)。病巣が小さく、他への転移がない場合、適応となることがあります。通常の放射線治療に比較し周囲の正常組織への放射線量を極力減少させることが可能です。約1週間程度通院、もしくは入院していただき治療を行います。手術に比べると症例数は少ないですが、90%前後の腫瘍制御が期待されます。
- 通常の放射線治療
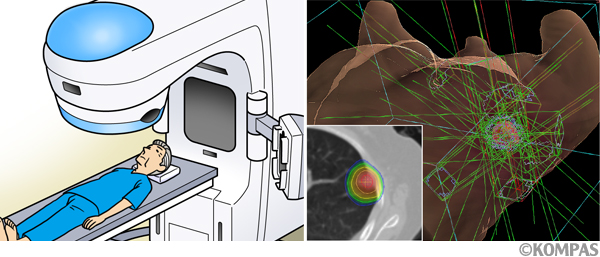
図1. 定位的放射線治療のコンピュータイメージ
- 薬物療法
- 適応:基本的には手術や放射線療法が適応とならない、肺がん患者さんが対象となりますが、上述のように術後に補助的に行う場合や放射線との併用を行う場合もあります。いずれにしても化学療法に用いる抗がん剤は、少なからず副作用を伴うため、適応となるのは全身状態が良好な患者さんです。抗がん剤の副作用で、逆に生活の質を落としてしまったり、寿命を縮めたりしてしまう可能性があるからです。高齢の方であっても全身状態が良ければ適応はありますが、抗がん剤の選択を含め注意が必要です。
- 薬剤の選択:これまでに化学療法を受けたことがない肺がん患者さんにおける標準的な化学療法(一次治療)は、プラチナ製剤と1990年以降に開発された新規の抗がん剤との2剤を用いた併用療法です。一次治療が無効な場合や、有効であってもその後に再発した場合には、二次治療、三次治療を行うこともあります。薬剤としては抗がん剤のほかに、新しい分子標的治療薬(がん細胞に特異的に存在している物質を標的とした薬剤)であるイレッサ®、タルセバ®、ジオトリフ®、タグリッソ®(EGFR遺伝子変異を伴う肺がん)、ザーコリ®、アレセンサ®、ジカディア®(EML4-ALK染色体転座を伴う肺がん)や)、タフィンラー®とメキニスト®(BRAF V600E遺伝子変異を伴う肺がん)アバスチン®、サイラムザ®(血管内皮増殖因子に対する抗体薬)なども、がんの特徴に応じて使用されます。また最近開発の著しい免疫チェックポイント阻害薬は、がん細胞により抑制されている自己の免疫を再活性化させることで、がん細胞を攻撃できるようにする薬剤です。肺がんで使用できるものは、オプジーボ®、キイトルーダ®、テセントリク®、イミフィンジ®があります。他の抗がん剤と組み合わせて、使用することもあります。イミフィンジ®は、局所進行型のIII期非小細胞肺がんに対して、化学放射線療法の後に追加することで、効果を発揮します。
- 成績:手術および放射線治療ができないと判断された進行した非小細胞肺がんであっても、近年の新しい治療法の開発により5年を超える生存期間を得ている患者さんもいらっしゃいます。ただし、上に示したように薬の適応は個々の患者さんで異なりますので、専門医による慎重な判断が必要となります。
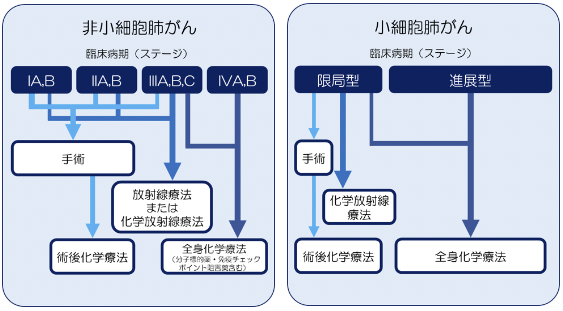
図2. 肺がんの病期(ステージ)別治療
(※ 実際の治療には、患者さんの病状や他の要素も多々影響します。)
生活上の注意
肺がんの最大の要因は喫煙であり、禁煙は何より重要な予防法です。肺がんにかかってから禁煙を行っても、寿命を延長する効果があるという報告もあります。当院では禁煙外来(木曜午後:舘野)も開設していますので、ご希望の方はぜひお問い合わせください。
また、間質性肺炎など呼吸器の病気を持っている方も肺がんを発症しやすいので、肺がんの早期発見のためにも、定期的な外来受診を続けてください。
慶應義塾大学病院ならではの取り組み
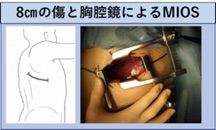
呼吸器外科では、8cmの傷に胸腔鏡を併用した低侵襲手術(Minimally Invasive Open Surgery: MIOS)で肺がん手術を行っています。これは、1) 安全性(合併症なく退院できること)、2) 根治性(肺がんを取り切れること)、3) 低侵襲性(体への負担が少ないこと)の3要素のバランスが最も取れた術式です。また、当院は総合病院であるため、術後に一定の頻度で発生する合併症(間質性肺炎、心疾患、脳血管障害など)に対しても各疾患の専門家と連携して迅速な対応をとることが可能です。実際に、肺がん術後の手術死亡率は全国平均で0.4%ありますが、当院では淺村教授が就任した2015年以降0%を継続しています(2019年8月現在)。また、がんによって気管や気管支が狭くなってしまった患者さんには気管支鏡を使った治療(ステント治療)も積極的に行っています。
呼吸器内科では、抗がん剤の使用に関しては、より安全で効果の高い使用方法を見つけるために、ほかの関連施設と協力して、いくつかの臨床試験、薬剤治験を行っています。また、がんゲノム中核拠点病院として、がん遺伝子パネル検査(保険診療)を行っています。腫瘍センターがん遺伝子外来でがん遺伝子パネル検査 PleSSion検査(自費診療)も行っておりますので、ご希望される患者さんは担当医にお申し出ください。
放射線治療では、積極的に強度変調放射線療法(IMRT)を用いることで、腫瘍周囲の肺や心臓といった正常臓器への照射線量を軽減し、治療に伴う有害事象を減らせるように努めています。
さらに詳しく知りたい方へ
-
日本肺癌学会

「肺癌診療ガイドライン」が公開されており、ほぼ毎年更新されています。